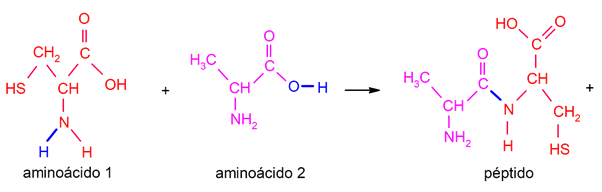
Los enlaces peptídicos son un tipo específico de vínculo entre un aminoácido y otro, que toma lugar a través de un grupo amino (-NH2) en el primer aminoácido y un grupo carboxilo (-COOH) en el segundo, produciendo un enlace covalente -CO-NH- y liberando una molécula de agua. Por ejemplo: oxitocina, vasopresina, leptina.
De esta manera se obtiene una nueva molécula llamada péptido y que llevará el nombre de ambos aminoácidos. El enlace peptídico entre una molécula de alanina (que aporta el terminal -NH2) y otra de serina (que aporta el terminal -COOH) se nombra como un péptido alanil-serina.
Esta es una de las formas de vínculo que permiten juntar aminoácidos (mediante deshidratación) para producir estructuras más complejas (polipéptidos) ya que una vez obtenido el enlace, es posible seguir uniendo aminoácidos mediante el mismo proceso, a partir del grupo carboxilo terminal. De esta misma manera, se pueden obtener estructuras más complejas como los polipéptidos y las proteínas. Es un procedimiento sumamente común en los seres vivos.
Propiedades de los enlaces peptídicos
Los enlaces peptídicos tienen ciertas características. Por ejemplo, el nexo establecido es de tipo simple pero más corto: con características de un enlace doble, como estabilizarse por resonancia. Esto último impide giros libres en torno al enlace (algo común en este tipo de uniones), lo que le otorga al enlace peptídico una estructura plana inevitable.
De manera semejante, los enlaces peptídicos pueden degradarse o romperse mediante hidrólisis (añadidura de agua), liberando una cantidad de energía en un proceso muy lento. Este proceso puede acelerarse en presencia de catalizadores ácidos, básicos o enzimáticos.
Ejemplos de enlaces peptídicos
Cualquier péptido es un ejemplo perfecto de los enlaces peptídicos, ya que son el resultado de este tipo de juntura de aminoácidos. A continuación algunos de los más importantes:
- Bradiquinina (Arg-Pro-Pro-Gly-Phe-Ser-Pro-Phe-Arg). Compuesto por nueve aminoácidos, este péptido es un fármaco que produce vasodilatación y caída de la presión sanguínea, por lo que se usa para el tratamiento de los hipertensos.
- Oxitocina (Cys-Tyr-Ile-Gln-Asn-Cys-Pro-Leu-Gly). Es una hormona producida por el hipotálamo y que cumple funciones neuromoduladoras del sistema nervioso central y un rol vital en la preparación del cérvix femenino durante el parto y de los pechos durante la lactancia.
- Glucagón (NH2-His-Ser-Gln-Gly-Thr-Phe-Thr-Ser-Asp-Tyr-Ser-Lys-Tyr-Leu-Asp-Ser-Arg-Arg-Ala-Gln-Asp-Phe-Val-Gln-Trp-Leu-Met-Asn-Thr-COOH). Es una hormona peptídica de 29 aminoácidos que se sintetiza en el páncreas y que interviene en el metabolismo de los azúcares.
- Glutatión (L-γ-glutamil-L-cisteinilglicina). Es un tripéptido de tres aminoácidos: cisteína, glutamato y glicina. Es el principal antioxidante celular, que protege las células de radicales libres y peróxidos.
- Vasopresina (NH2-Cys-Tyr-Phe-Gln-Asn-Cys-Pro-Arg-Gly-COOH). Segregada por el hipotálamo, controla la reabsorción de las moléculas de agua de la orina, aumenta su concentración y cumple un papel clave como regulador homeostático sanguíneo. Es una hormona de nueve aminoácidos.
- Insulina. Es una hormona polipeptídica formada por 51 aminoácidos, segregada por el páncreas para regular el ciclo de los azúcares en sangre.
- Prolactina. Es una hormona peptídica que estimula la producción de leche en los pechos maternos. Se compone de una secuencia de 198 aminoácidos.
- Leptina. Es otra hormona peptídica que suprime la sensación de hambre y está compuesta por una cadena de 167 aminoácidos.
- Gastrina. Es una hormona peptídica que regula la producción de jugos gástricos en el estómago. Se compone de 14 aminoácidos.
- Pepsina. Es una hormona compuesta de 326 aminoácidos, encargada de regular los procesos de digestión y absorción de los alimentos.
Sigue con:
¿Te fue útil esta información?
Sí No¡Genial! gracias por visitarnos :)