Índice
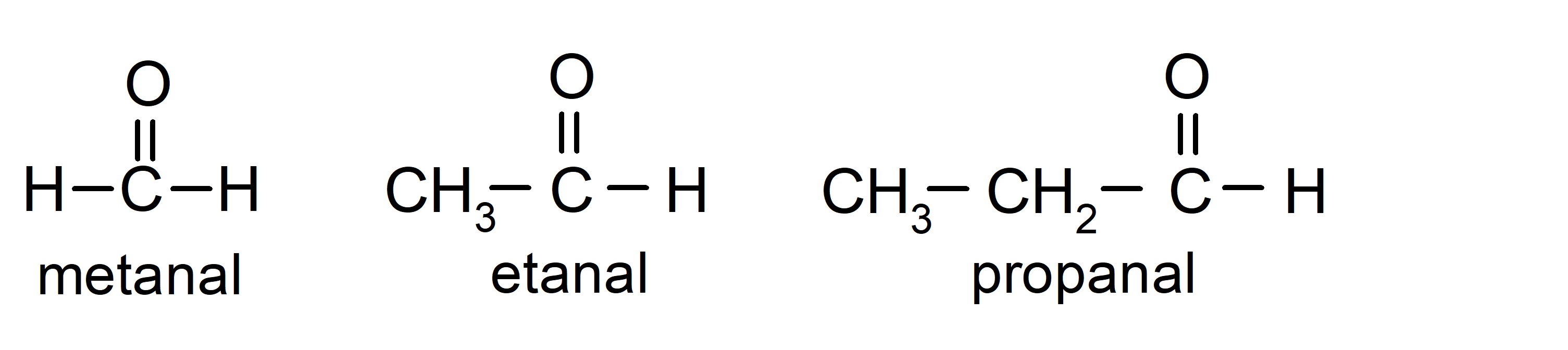
Los aldehídos son compuestos orgánicos que tienen en su estructura un grupo funcional carbonilo (= C = O) que está enlazado a una cadena carbonada y a un átomo de hidrógeno. Por ejemplo: el metanal (también llamado formaldehído), el etanal (también llamado acetaldehído) y el propanal (también llamado propaldehído).
Las cetonas son compuestos orgánicos que tienen en su estructura un grupo carbonilo enlazado a dos átomos de carbono. Por ejemplo: la propanona (también llamada acetona), la butanona y la 2-pentanona.
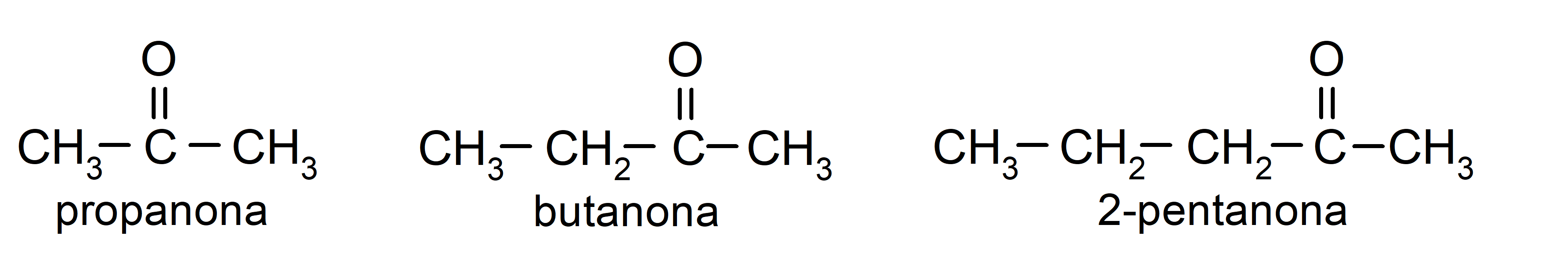
Diferencias entre aldehídos y cetonas
Las principales diferencias entre aldehídos y cetonas son:
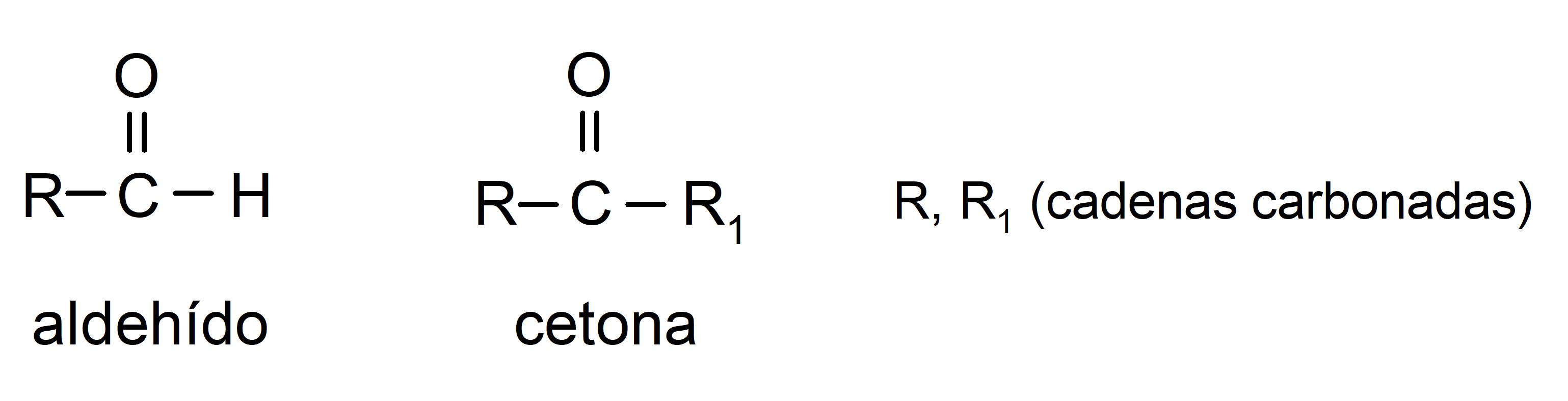
- Los aldehídos tienen en su estructura un grupo funcional carbonilo ubicado en un extremo terminal, mientras que las cetonas tienen el grupo carbonilo ubicado en posiciones no terminales de su estructura.
- Los aldehídos se oxidan por reacción con el reactivo de Tollens, formando plata metálica. También se oxidan frente al reactivo de Benedict, formando óxido cuproso. Las cetonas no se oxidan con ninguno de los dos reactivos.
- Los aldehídos se reducen a alcoholes primarios, mientras que las cetonas se reducen a alcoholes secundarios.
Propiedades físicas
Propiedades físicas de los aldehídos
Las propiedades físicas de los aldehídos son muy diversas debido a que dependen de la constitución de la cadena carbonada que está enlazada al grupo carbonilo.
Algunas son:
- Los aldehídos más solubles en agua son los que tienen menor tamaño, como el metanal y el etanal.
- Los aldehídos volátiles tienen olores penetrantes e incluso irritantes.
- El grupo carbonilo les confiere polaridad.
- Suelen tener puntos de ebullición más altos que compuestos químicos de tamaño molecular similar.
Propiedades físicas de las cetonas
Las propiedades físicas de las cetonas dependen de cómo está formada la cadena carbonada que está enlazada al grupo carbonilo.
- Muchas cetonas tienen olores agradables.
- Su solubilidad en agua depende del tamaño de la cadena carbonada unida al grupo carbonilo. Mientras más pequeña es la cadena carbonada, más soluble será la cetona en agua.
- El grupo carbonilo les confiere una polaridad acentuada.
- Tienen puntos de ebullición bastante altos en comparación con compuestos químicos de tamaño molecular comparable.
Propiedades químicas
Propiedades químicas de los aldehídos
Entre las propiedades químicas de los aldehídos podemos encontrar:
Se oxidan para formar el ácido carboxílico correspondiente, es decir, el ácido formado tendrá el mismo número de carbonos en la cadena carbonada que el aldehído que le dio origen. Por ejemplo:
- La oxidación con el reactivo de Tollens (complejo de plata amoniacal en solución básica, [Ag(NH3)2]+) del etanal produce ácido etanoico y plata metálica..
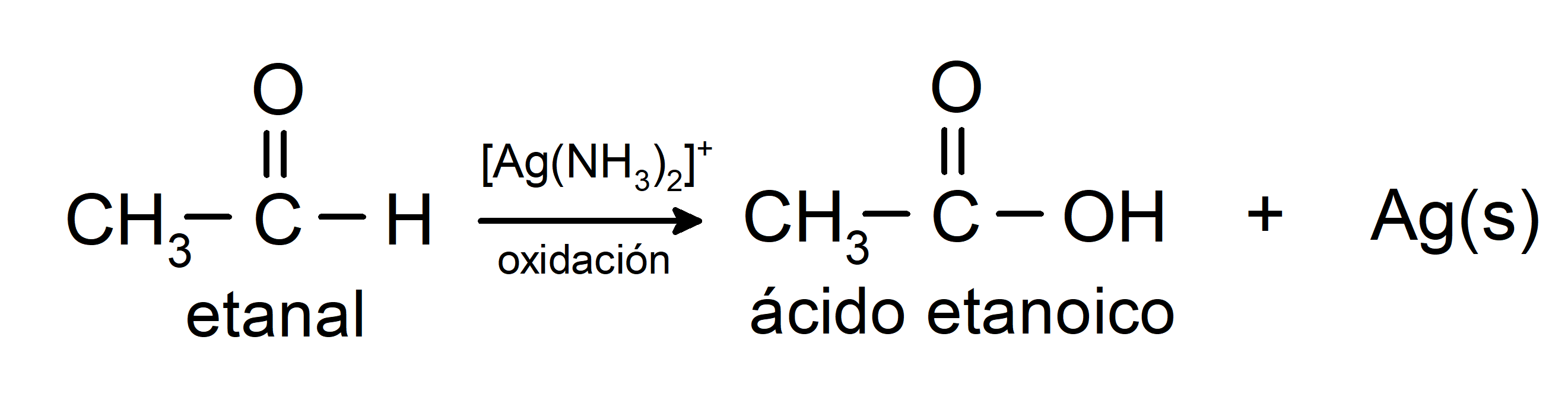
- La oxidación con el reactivo de Benedict (solución alcalina de sulfato de cobre) del etanal produce ácido etanoico y óxido cuproso.
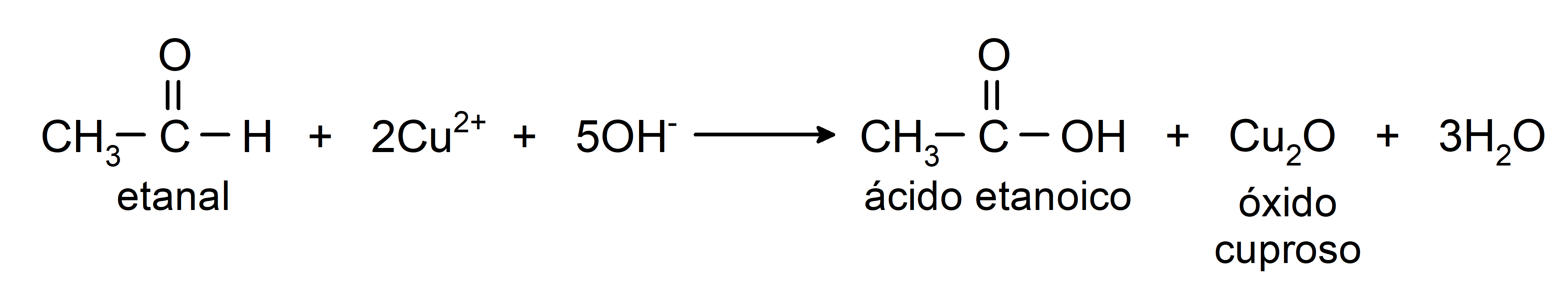
Experimentan reacciones de adición nucleofílica, es decir, adición de un nucleófilo al grupo carbonilo. Por ejemplo:
- Adición de ácido cianhídrico para formar cianhidrinas o cianohidrinas.
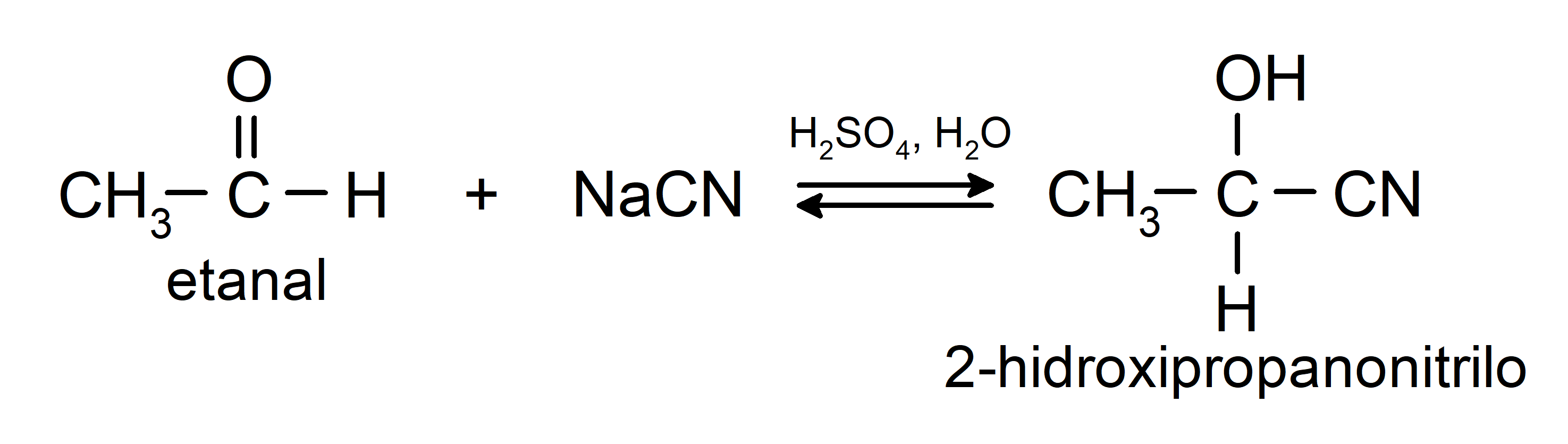
- En presencia de ácidos anhidros, se adicionan alcoholes al grupo carbonilo de los aldehídos para formar acetales y hemiacetales.
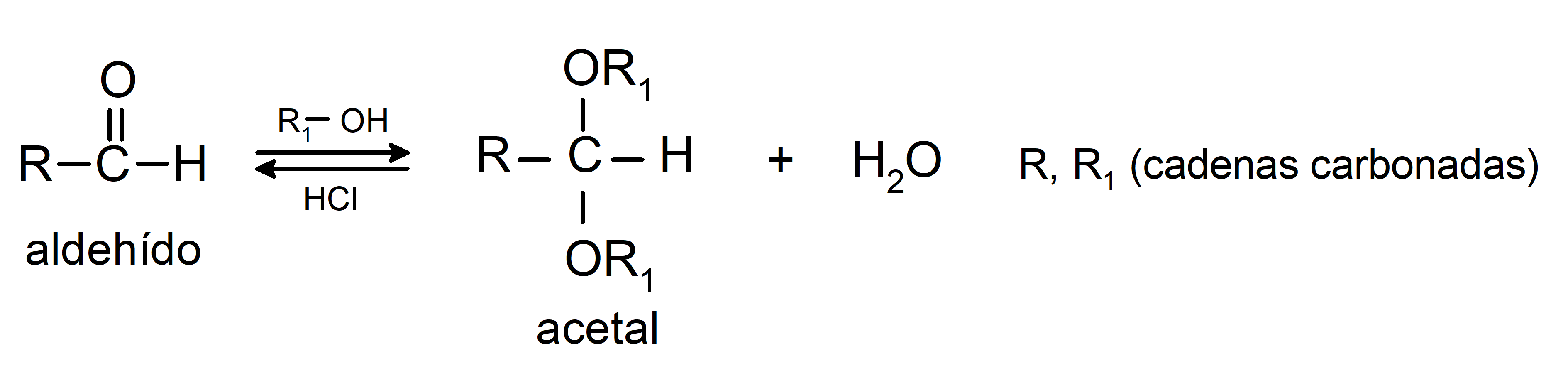
Experimentan reacciones de condensación aldólica. En estas reacciones se produce la unión de dos aldehídos en presencia de hidróxido de sodio (NaOH) y el compuesto químico resultante se llama aldol. Por ejemplo:
- Reacción de condensación del etanal en presencia de NaOH diluido.
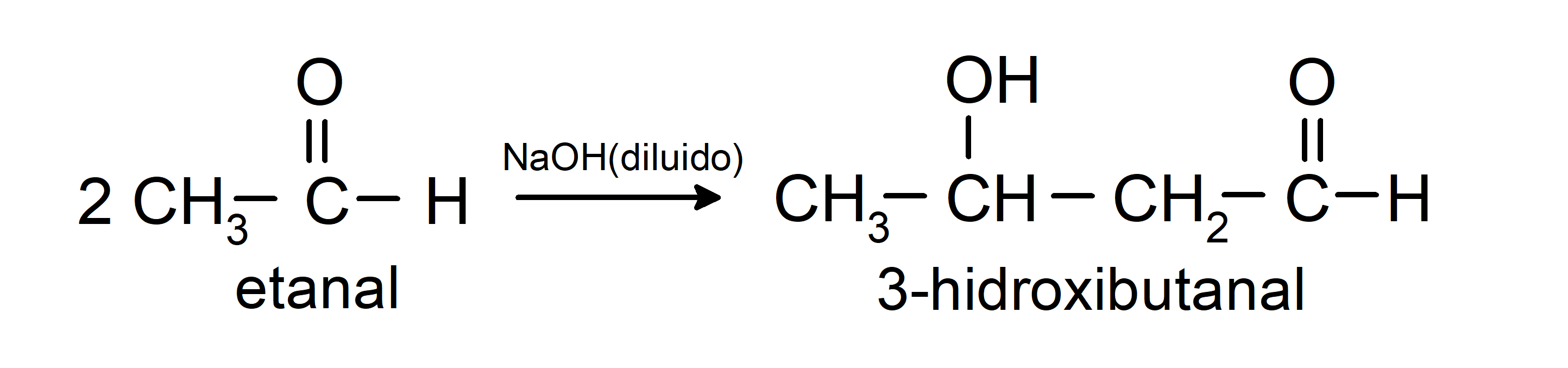
Se reducen a alcoholes primarios. Los aldehídos se pueden reducir a alcoholes primarios por hidrogenación catalítica o por reducción con borohidruro de sodio (NaBH4) e hidruro de litio y aluminio (LiAlH4).
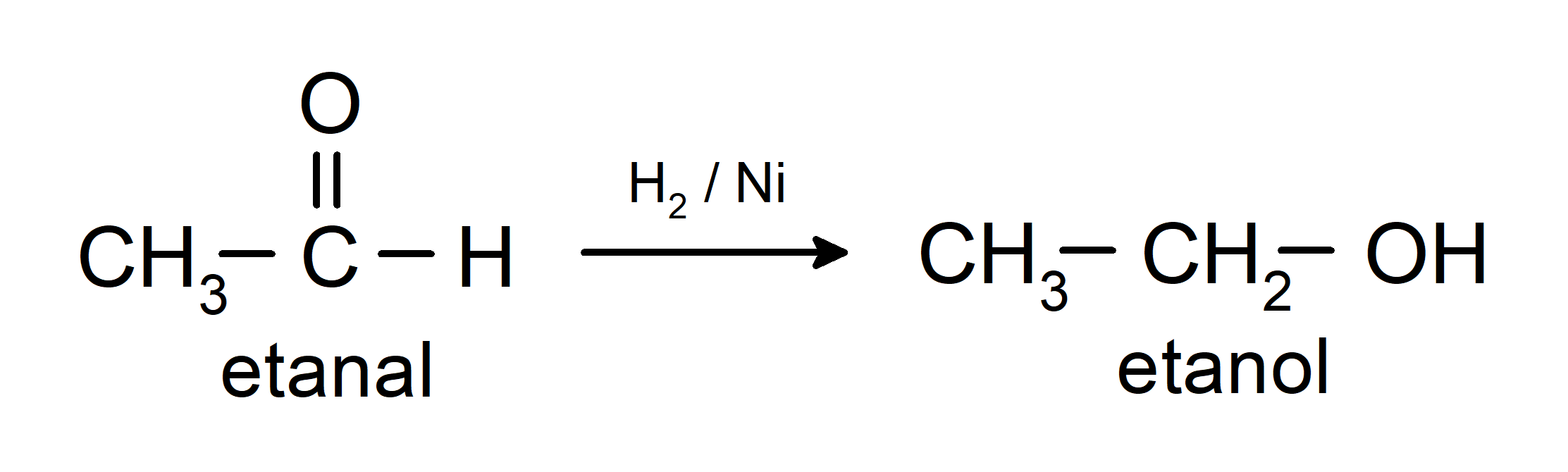
Propiedades químicas de las cetonas
Entre las propiedades químicas de las cetonas podemos encontrar:
Experimentan reacciones de adición nucleofílica. Por ejemplo:
- Adición de ácido cianhídrico para formar cianhidrinas o cianohidrinas.
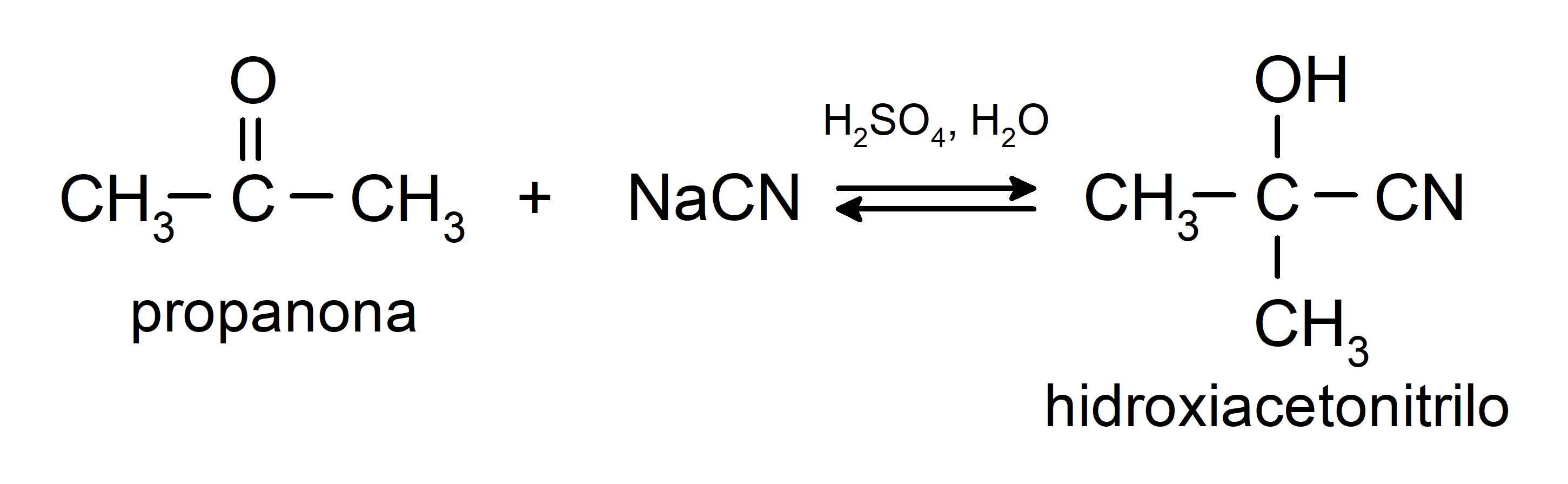
Adicionan alcoholes (en presencia de ácidos anhidros) al grupo carbonilo de las cetonas para formar cetales y hemicetales. Por ejemplo:
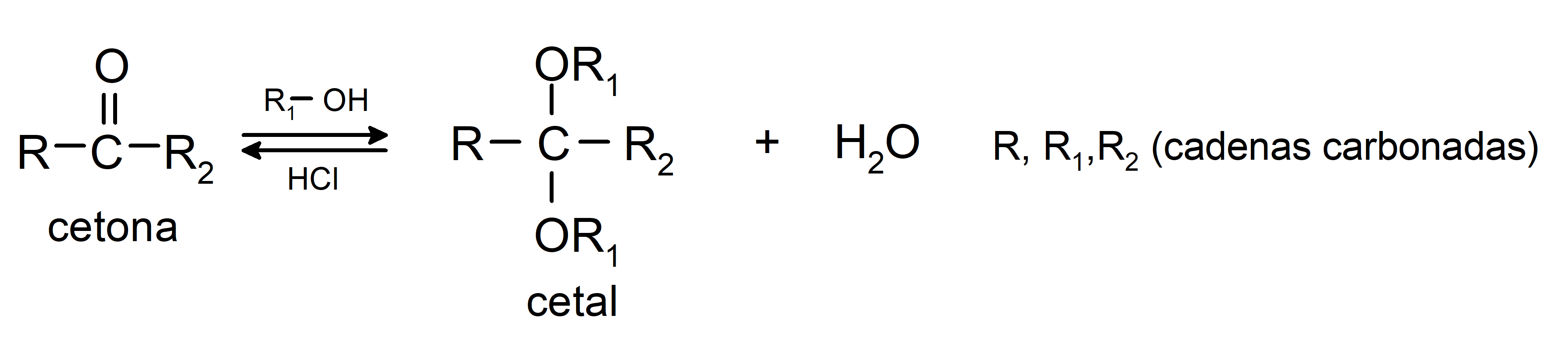
Experimentan reacciones de halogenación. Las cetonas que tienen un hidrógeno alfa (α) reaccionan por sustitución de este hidrógeno por halógenos (cloro (Cl), bromo (Br), yodo (I), flúor (F)) en presencia catalizadores ácidos o básicos. La sustitución se produce casi exclusivamente en el carbono α, es decir, el carbono que tiene unido al hidrógeno α. Por ejemplo:
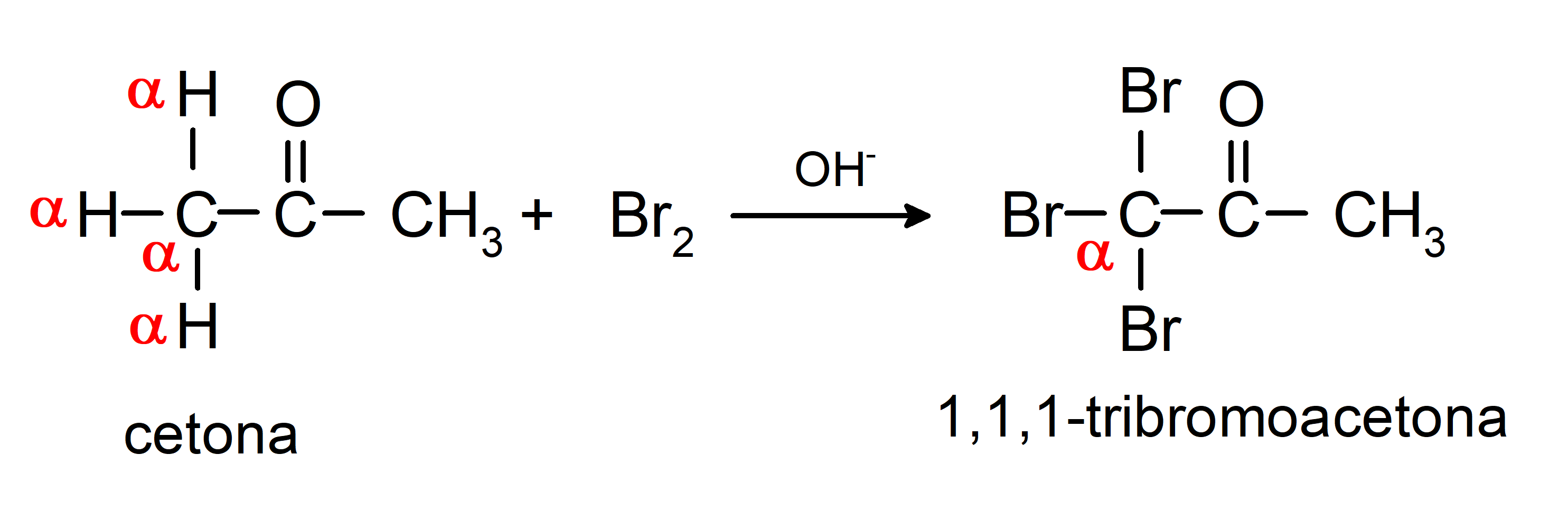
Se reducen a alcoholes secundarios por hidrogenación catalítica o por reducción con borohidruro de sodio (NaBH4) e hidruro de litio y aluminio (LiAlH4). Por ejemplo:
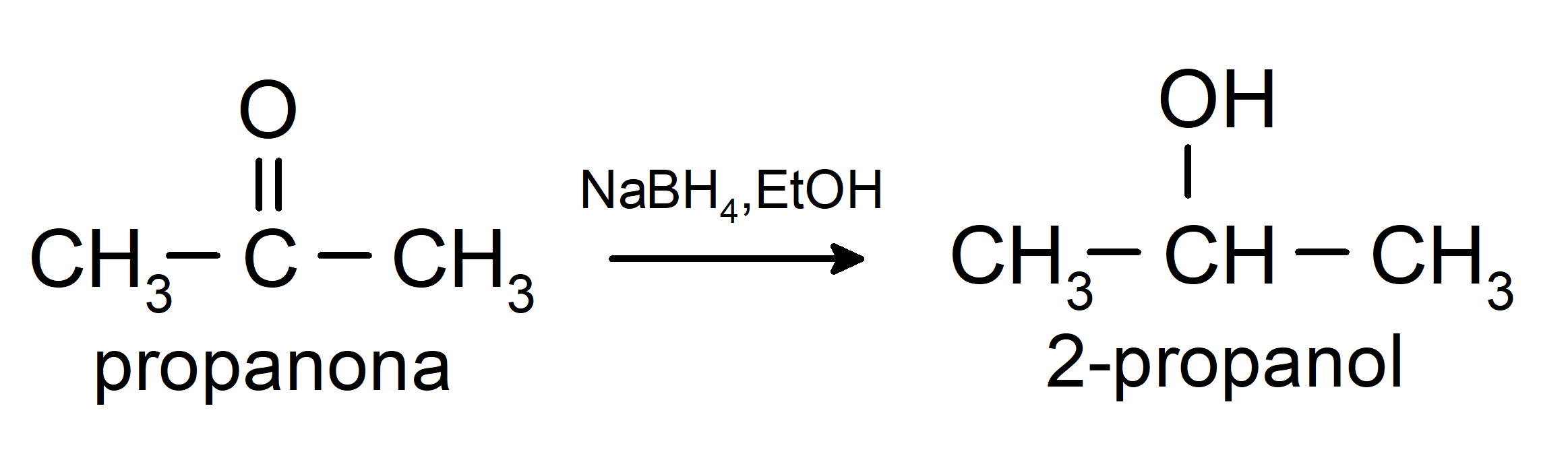
Las cetonas no se oxidan con los reactivos de Tollens y Benedict.
Nomenclatura de los aldehídos
Según las reglas establecidas por la Unión Internacional de Química Pura y Aplicada (IUPAC), los aldehídos se nombran utilizando prefijos que indican la cantidad de carbonos que tiene la cadena carbonada. No es necesario especificar la posición del grupo carbonilo, ya que siempre está en posición uno, en un extremo de la molécula. Además, se escribe el sufijo -al al final del nombre del aldehído. Por ejemplo:
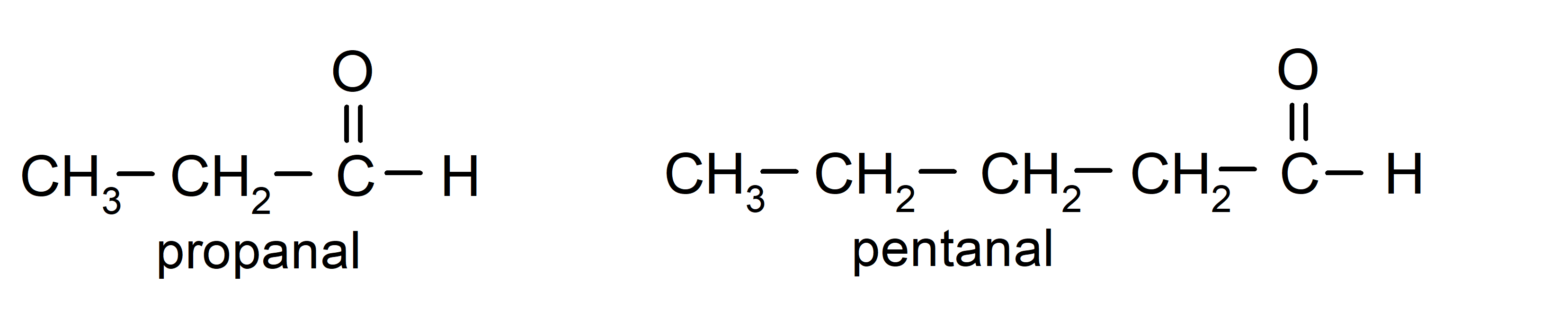
Si el aldehído está formado por varias cadenas carbonadas, o sea, que tiene ramificaciones, se elige como cadena principal la cadena carbonada con mayor cantidad de átomos de carbono. Las demás cadenas son nombradas como grupos sustituyentes, y la posición de cada sustituyente, se elige de forma que ocupe la menor numeración posible en la cadena. Además, se comienzan a contar los átomos de carbono empezando por el extremo que tiene el grupo carbonilo. Por ejemplo:
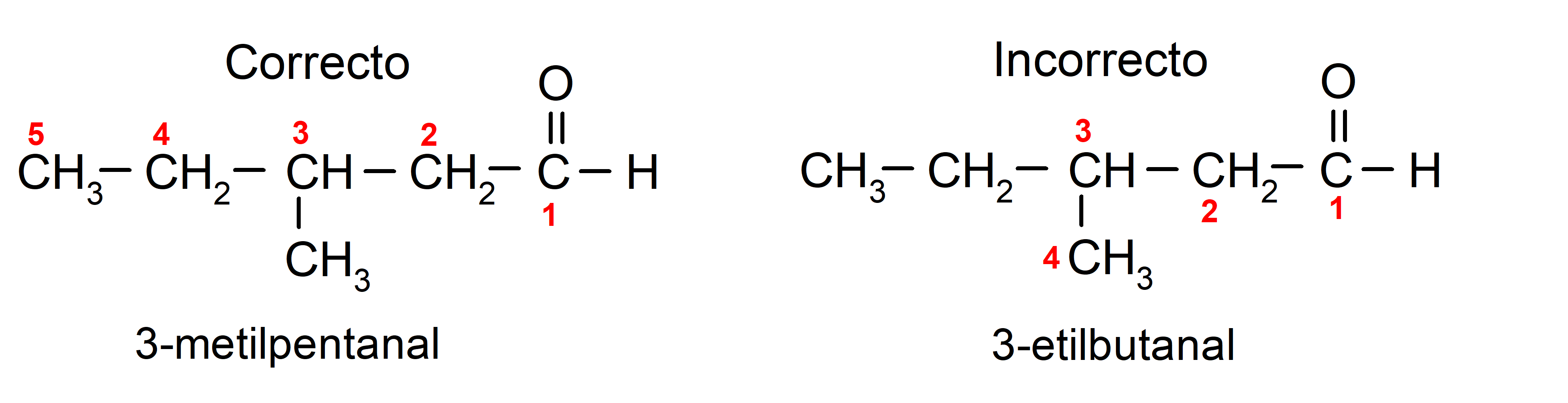
Los aldehídos que tienen dos grupos carbonilos se nombran utilizando el sufijo -dial. Por ejemplo:
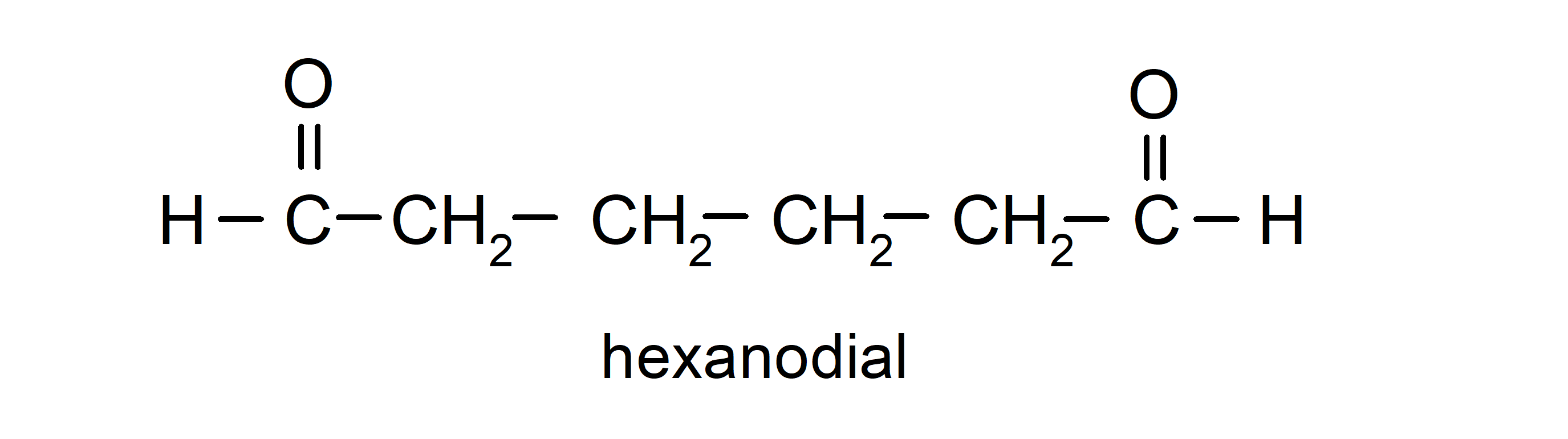
Nomenclatura de las cetonas
Según la Unión Internacional de Química Pura y Aplicada (IUPAC), las cetonas se nombran utilizando prefijos que indican la cantidad de carbonos que tiene la cadena carbonada.
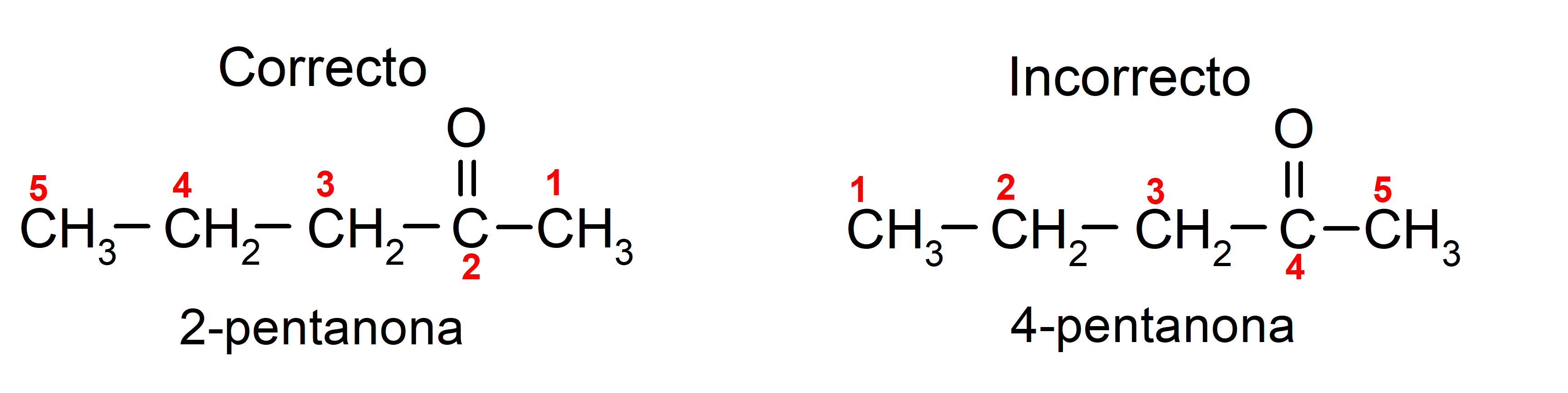
Por otra parte, se escribe el nombre de la acetona utilizando el sufijo -ona, precedido por un número que indica la posición del grupo carbonilo en la cadena carbonada. La ubicación del grupo carbonilo se debe elegir de tal forma que le corresponda a la menor numeración posible. Por ejemplo:
Para nombrar una cetona que está formada por varias cadenas carbonadas, es decir, con ramificaciones, se elige como cadena principal la cadena carbonada con mayor cantidad de átomos de carbono y que contiene al grupo carbonilo. El resto de las cadenas se nombran como grupos sustituyentes. Por ejemplo:
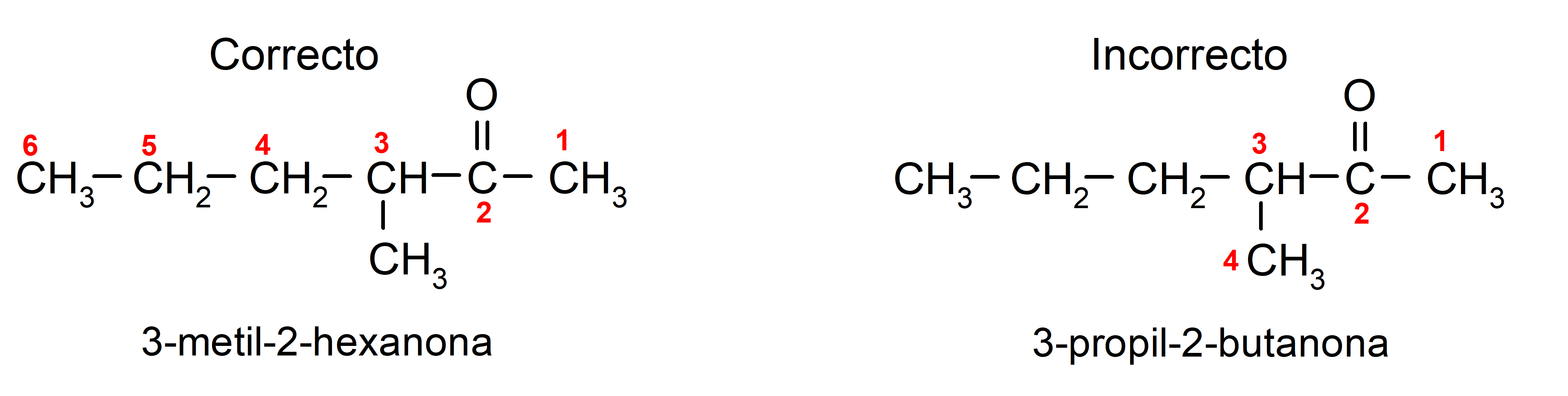
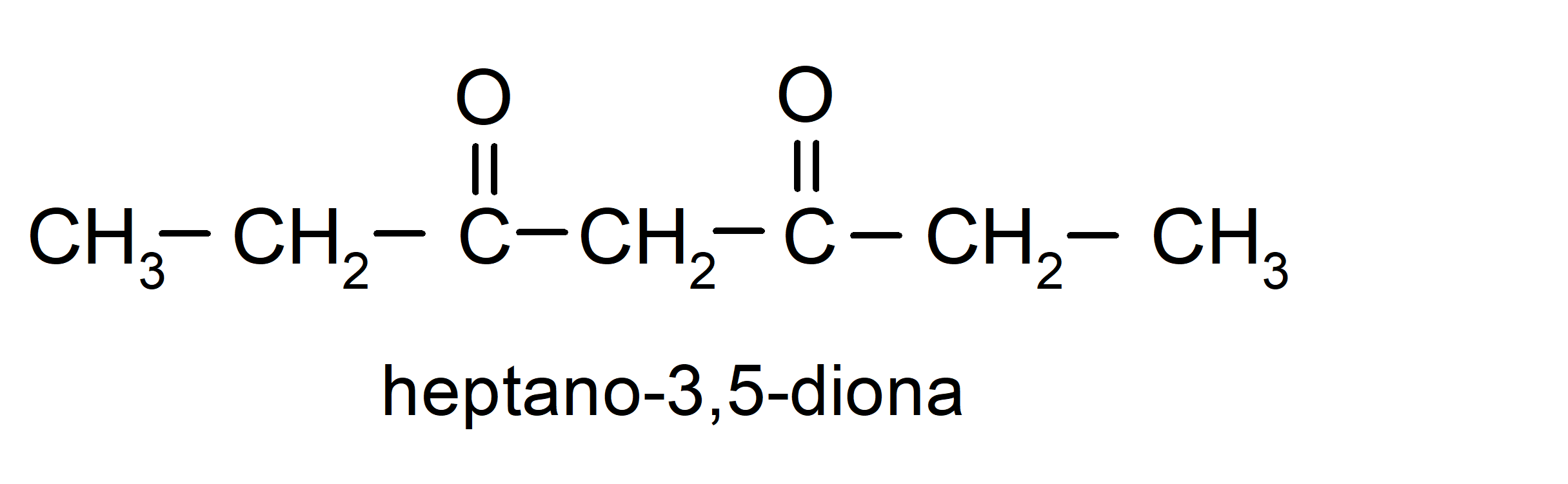
Existen cetonas que tienen dos grupos carbonilos, se denominan dionas. Por ejemplo:
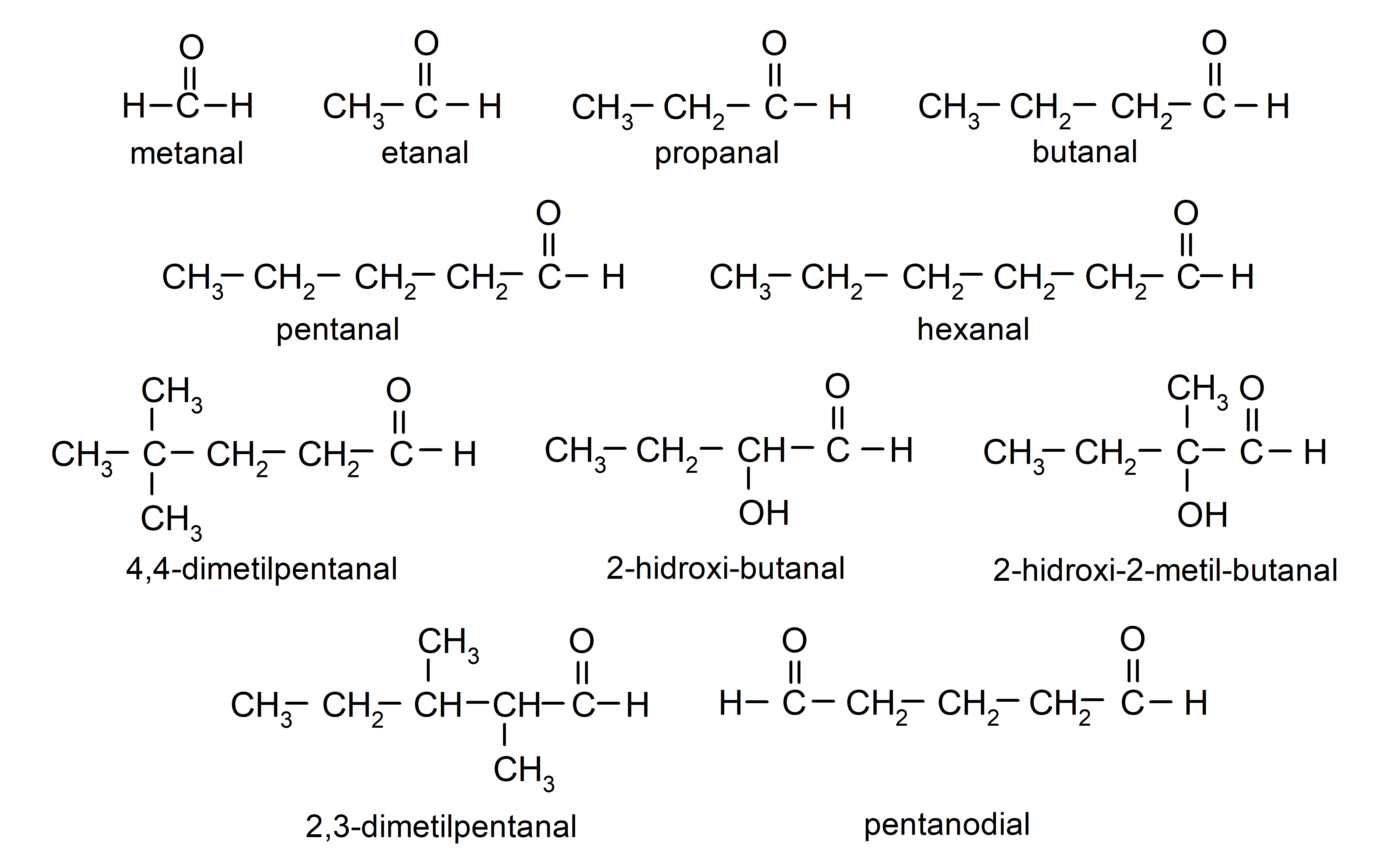
Ejemplos de aldehídos
- metanal (formaldehído)
- etanal (acetaldehído)
- propanal (propaldehído)
- butanal
- pentanal
- hexanal
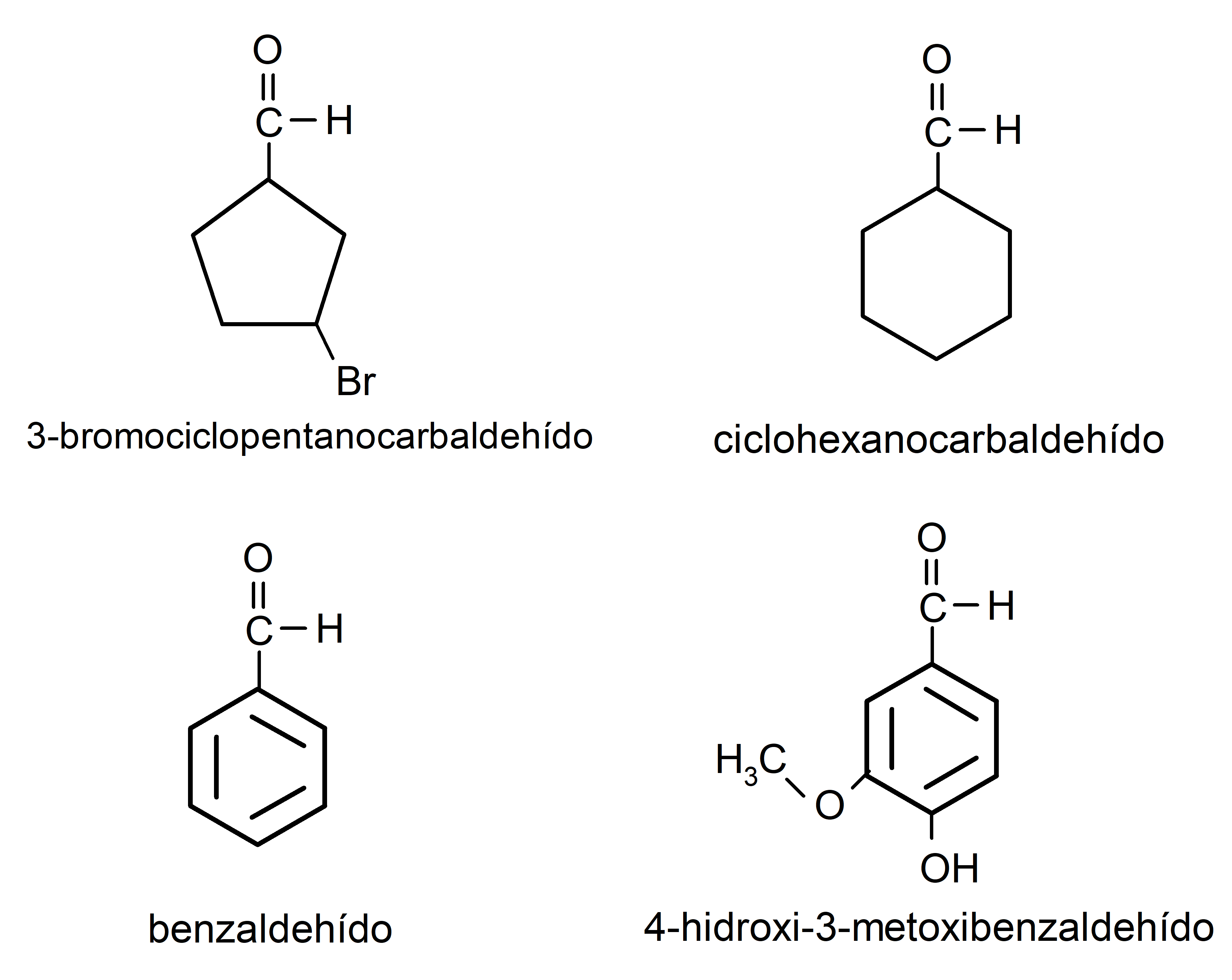
- 3-bromociclopentanocarbaldehído
- ciclohexanocarbaldehído
- benzaldehído
- 4,4-dimetilpentanal
- 2-hidroxi-butanal
- 2-hidroxi-2-metil-butanal
- 2,3-dimetilpentanal
- pentanodial
- 4-hidroxi-3-metoxibenzaldehído
Ejemplos de cetonas
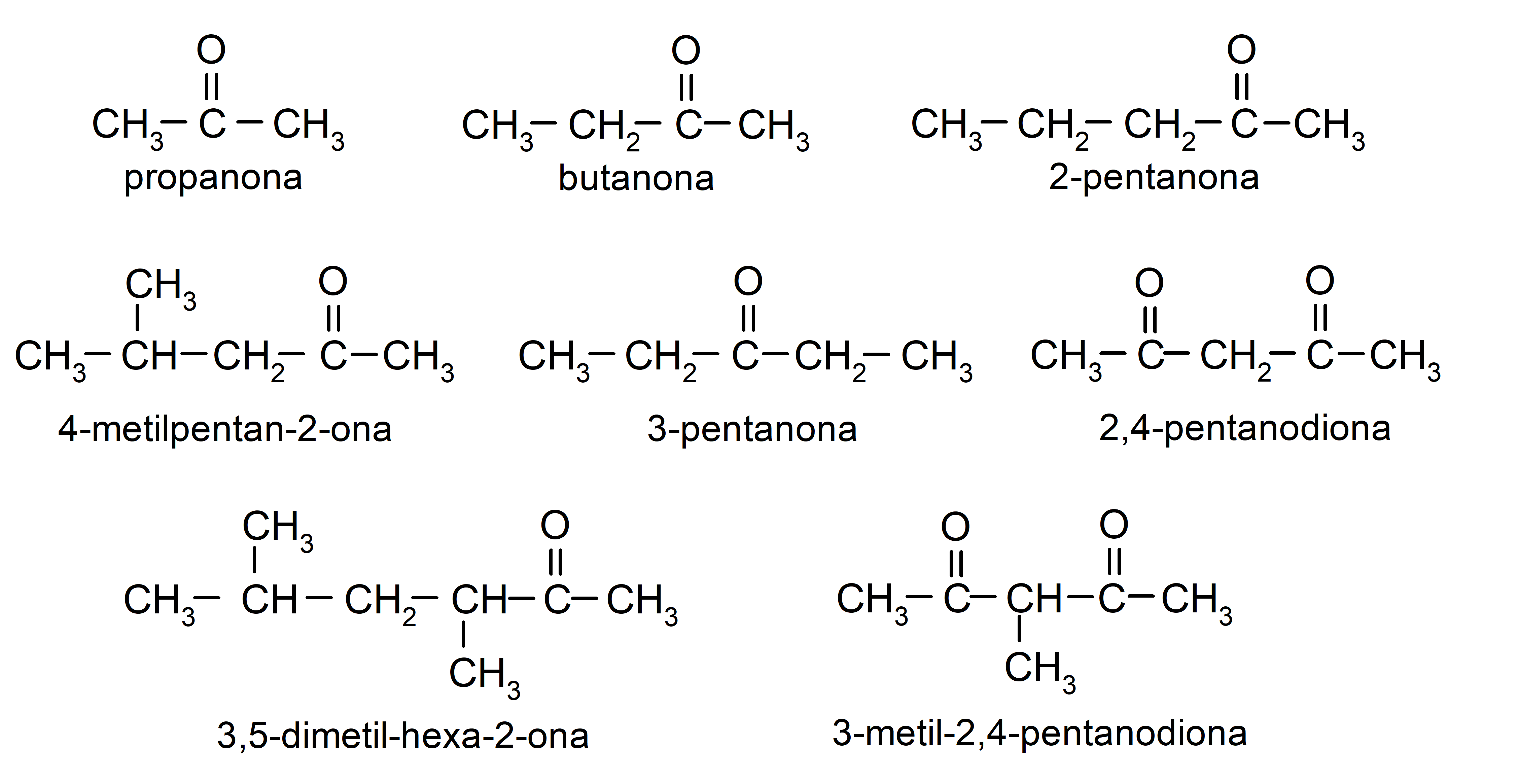
- propanona (acetona)
- butanona
- 2-pentanona
- 4-metilpentan-2-ona
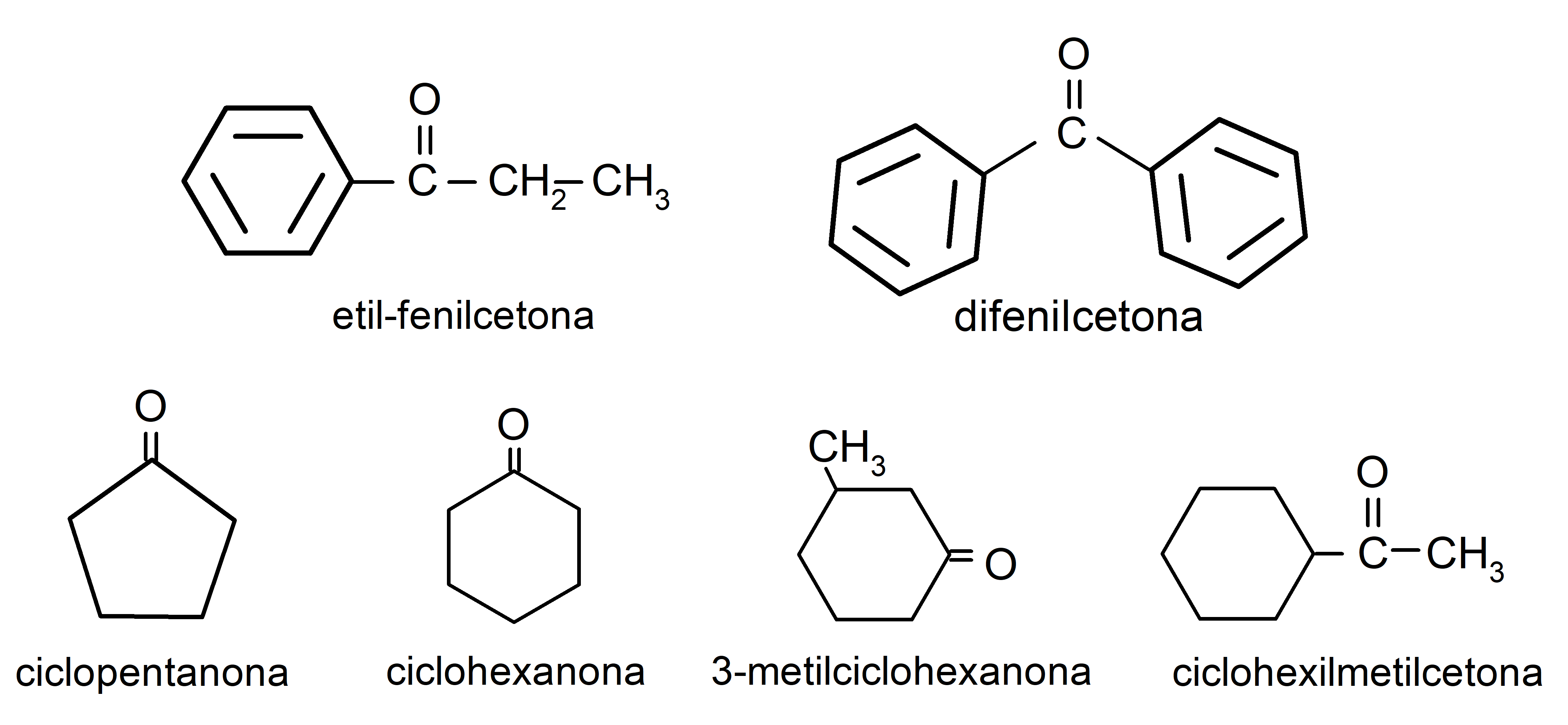
- 3-metilciclohexanona
- ciclohexilmetilcetona
- 3,4 dimetil-hexan-2-ona
- etil-fenilcetona
- 2,4-pentanodiona
- ciclohexanona
- 3-pentanona
- 3-metil-2,4-pentanodiona
- 1-fenilpropanona
- ciclopentanona
- difenilcetona
Usos de los aldehídos en la vida cotidiana
Algunos usos de los aldehídos son:
- Se utilizan para producir solventes, pinturas, perfumes, resinas y esencias.
- Se emplean como conservantes de productos cosméticos, de muestras biológicas y cadáveres. El formaldehído es el más utilizado con estos fines.
- Se usan para producir plásticos, que permiten la sustitución de piezas metálicas en la industria automovilística.
- Se utilizan como aromatizantes de algunos alimentos.
- Se utilizan como agentes desinfectantes.
- Se han utilizado para fabricar algunos explosivos, como el tetranitrato de pentaeritritol (TNPE).
Usos de las cetonas en la vida diaria
Algunos usos de las cetonas son:
- Se emplean en la producción de solventes. Especialmente la acetona es muy utilizada para remover pinturas y lacas.
- Se utilizan en la fabricación de algunos cauchos y lubricantes.
- Se usan para producir pinturas, lacas y barnices.
- Se utilizan para producir medicamentos y cosméticos.
Toxicidad de aldehídos y cetonas
- Los aldehídos. El contacto con aldehídos provoca irritación en la piel, en los ojos y en las vías respiratorias. Además, la exposición a aldehídos ha sido vinculada con enfermedades como cáncer, dermatitis de contacto y enfermedades hepáticas y neurodegenerativas. El formaldehído, por ejemplo, es considerado por la OMS (Organización Mundial de la Salud) un compuesto cancerígeno.
- Las cetonas. La exposición repetida a las cetonas puede ocasionar daños al sistema nervioso central. Esto puede generar pérdida de memoria, debilidad, dolores musculares y calambres. Además, si la piel entra en contacto con cetonas, se generan sequedad y grietas. Por otra parte, si se inhalan cetonas, se produce irritación de las vías respiratorias y tos.
Sigue con:
¿Te fue útil esta información?
Sí No¡Genial! gracias por visitarnos :)