Índice
Los alcoholes son compuestos químicos orgánicos que contienen en su estructura el grupo funcional hidroxilo (- OH) unido a un carbono (- C). Se denomina “carbinol” al grupo (- C – OH). Algunos ejemplos de alcoholes son: metanol, etanol y 1-propanol.
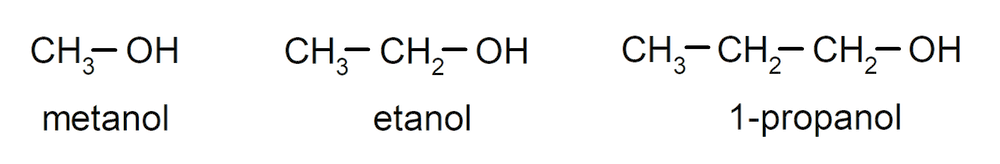
Los alcoholes son compuestos químicos con diversos usos en la vida cotidiana, pues tienen propiedades antibacterianas y antisépticas. Por otro lado, pueden ser peligrosos para la salud humana cuando se ingieren de forma descontrolada.
Igualmente, no todos los alcoholes pueden ser ingeridos por el ser humano.
Tipos de alcoholes
Según la cantidad de átomos de carbono a la que está unido el átomo de carbono que tiene unido el grupo hidroxilo, un alcohol puede ser:
- Alcohol primario. El átomo de carbono que tiene unido el grupo hidroxilo está unido además a un solo átomo de carbono. Por ejemplo:
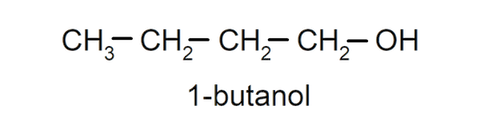
- Alcohol secundario. El átomo de carbono que tiene unido el grupo hidroxilo está unido además a otros dos átomos de carbono. Por ejemplo:
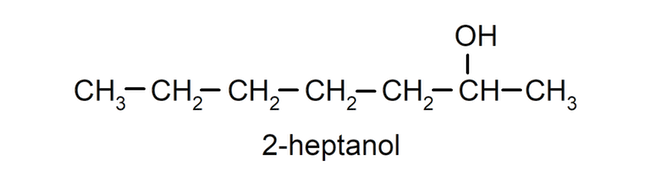
- Alcohol terciario. El átomo de carbono que tiene unido el grupo hidroxilo está unido además a tres átomos de carbono. Por ejemplo:
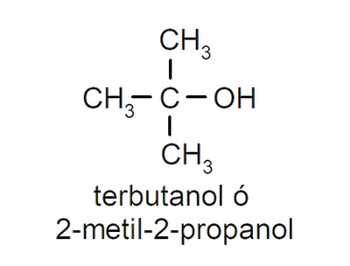
Según la cantidad de grupos hidroxilo que tiene, un alcohol puede ser:
- Diol. Tiene dos grupos hidroxilos en su estructura. Por ejemplo:
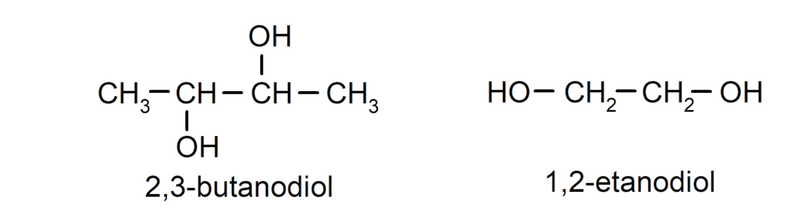
- Triol. Tiene tres grupos hidroxilos en su estructura. Por ejemplo:

- Polialcohol. Tiene muchos grupos hidroxilos en su estructura. Por ejemplo:
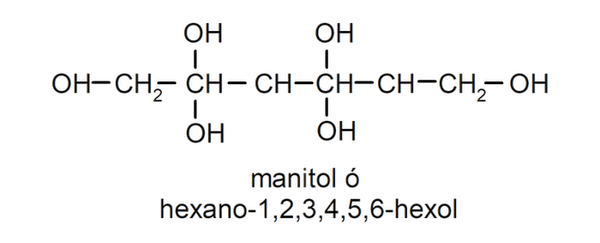
Propiedades físicas de los alcoholes
Algunas de las propiedades físicas de los alcoholes son:
- Punto de ebullición. El punto de ebullición en los alcoholes es bastante elevado debido a la presencia del grupo hidroxilo, que permite la formación de puentes de hidrógeno. Además, mientras más grupos funcionales hidroxilo estén presentes en la cadena carbonada, más elevado será el punto de ebullición de los alcoholes.
- Polaridad. Los alcoholes son compuestos bastante polares.
- Solubilidad. Los alcoholes de bajo peso molecular son solubles en agua. Por otra parte, mientras más grande sea la cadena carbonada de los alcoholes, menor será su solubilidad en agua. Además, mientras más grupos hidroxilos tengan los alcoholes, mayor será su solubilidad en agua.
- Estado de agregación. La mayoría de los alcoholes son líquidos a temperatura ambiente (25 ºC) y tienen olores característicos.
Propiedades químicas de los alcoholes
Algunas de las propiedades químicas de los alcoholes son:
- Los alcoholes se comportan como ácidos y como bases. Su comportamiento como ácidos se puede ver en reacciones con metales activos para liberar hidrógeno gaseoso y formar alcóxidos.
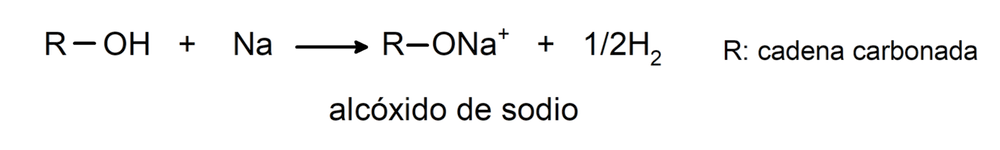
Su comportamiento como bases se puede ver en reacciones como la reacción del metanol con bromuro de hidrógeno para formar bromuro de metiloxonio.
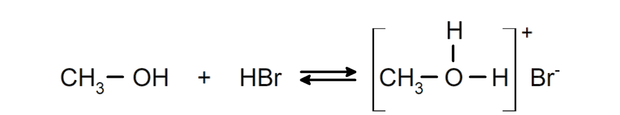
- Los alcoholes experimentan reacciones de halogenación. Reaccionan con halogenuros de hidrógeno para formar halogenuros de alquilo.
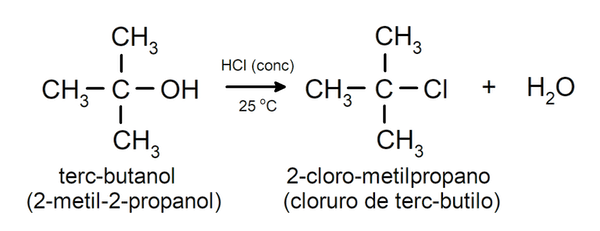
- Los alcoholes experimentan reacciones de oxidación cuando reaccionan con determinados compuestos oxidantes. Los productos de las reacciones de oxidación dependen del tipo de alcohol que reacciona, es decir, si es primario, secundario o terciario.
Oxidación de alcohol primario para formar aldehído o ácido carboxílico.
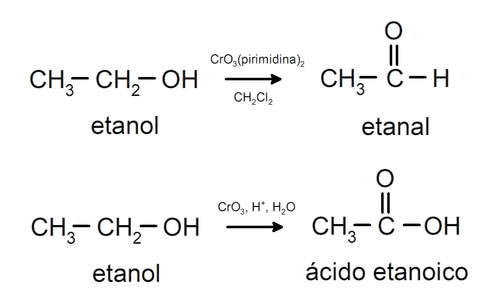
Oxidación de alcohol secundario para formar cetona.
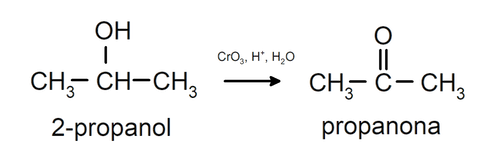
Los alcoholes terciarios no se oxidan con oxidantes comunes. Con agentes oxidantes muy fuertes se pueden transformar en alquenos, que luego pueden oxidarse.
Los alcoholes que tienen dos grupos hidroxilo ubicados en carbonos adyacentes se oxidan con tetraacetato de plomo para formar dos cetonas.
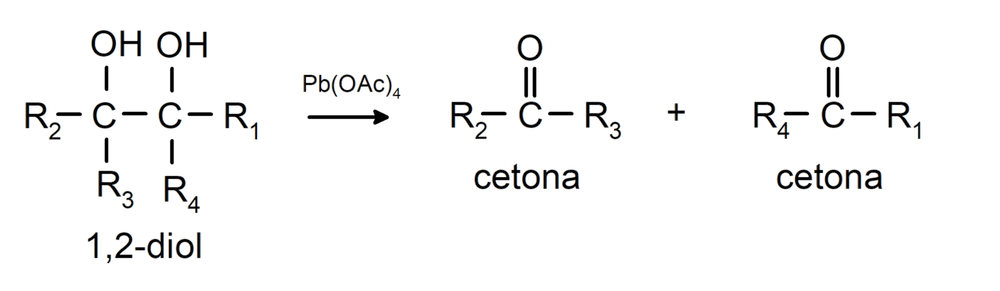
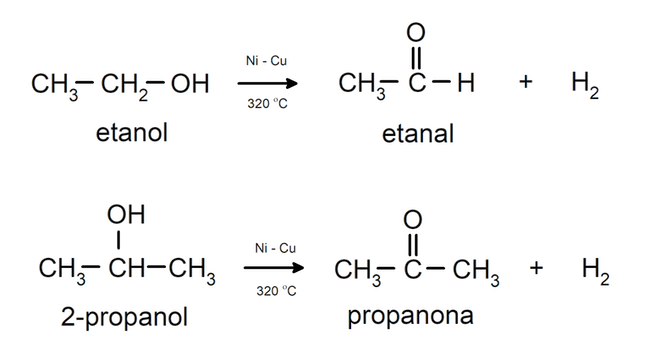
- Los alcoholes experimentan reacciones de deshidrogenación. Estas reacciones ocurren solo con alcoholes primarios y secundarios, que cuando son sometidos a altas temperaturas en presencia de catalizadores, liberan hidrógenos.
- Los alcoholes experimentan reacciones de deshidratación. Los alcoholes se deshidratan para formar los alquenos correspondientes. Esta reacción ocurre en presencia de ácido y temperaturas intermedias.
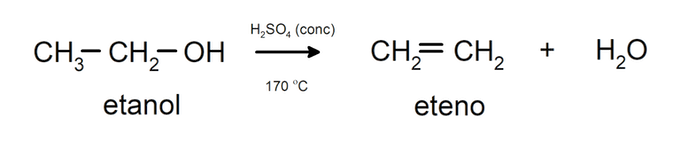
Nomenclatura de alcoholes
Según la nomenclatura establecida por la IUPAC (Unión Internacional de Química Pura y Aplicada), los alcoholes se nombran siguiendo las siguientes reglas:
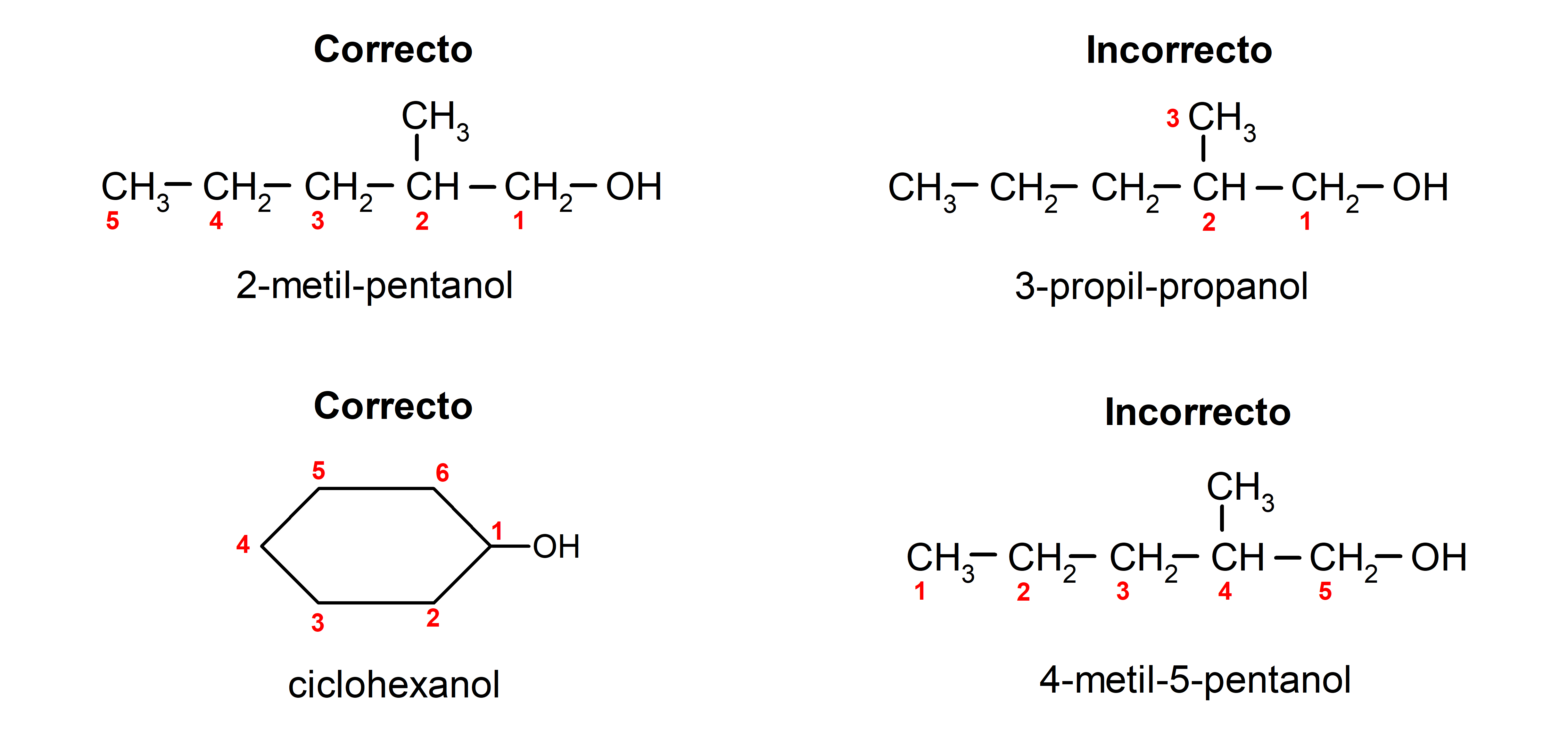
- Se elige la posición del grupo hidroxilo teniendo en cuenta que ocupe la menor numeración posible en la cadena carbonada. Si la estructura del alcohol es cíclica, se considera la posición 1 en el carbono que tiene unido el grupo hidroxilo y para nombrarlo se utiliza el prefijo ciclo-.
- El nombre del alcohol se escribe utilizando prefijos que indican la cantidad de átomos de la cadena carbonada, y además, se coloca el sufijo -ol.
- Si la estructura del alcohol tiene ramificaciones, se elige como cadena carbonada principal la cadena más larga y que además contenga el grupo hidroxilo.
Según la nomenclatura Tradicional, los alcoholes se nombran escribiendo la palabra “alcohol” y luego escribiendo el nombre del alcano correspondiente a la cadena carbonada, pero en lugar de utilizar la terminación -ano del alcano, se utiliza la terminación -ílico.
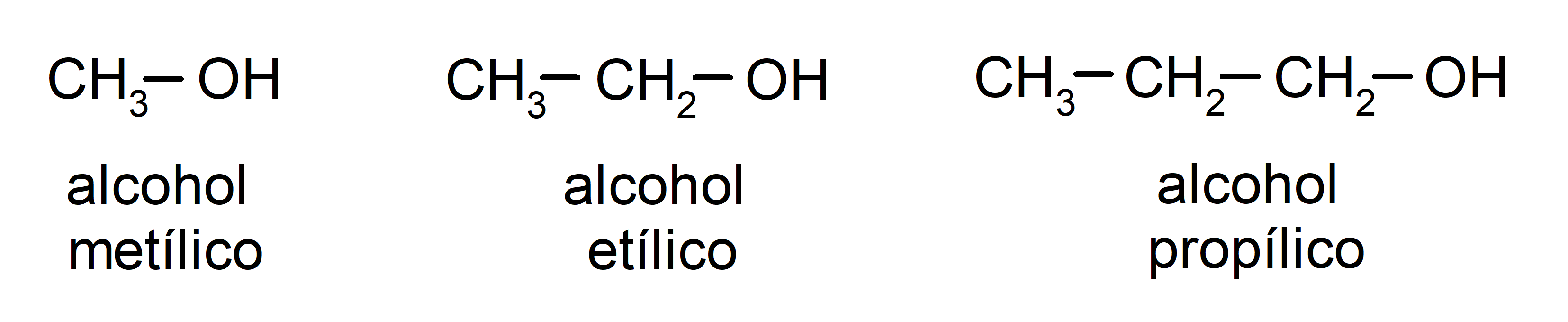
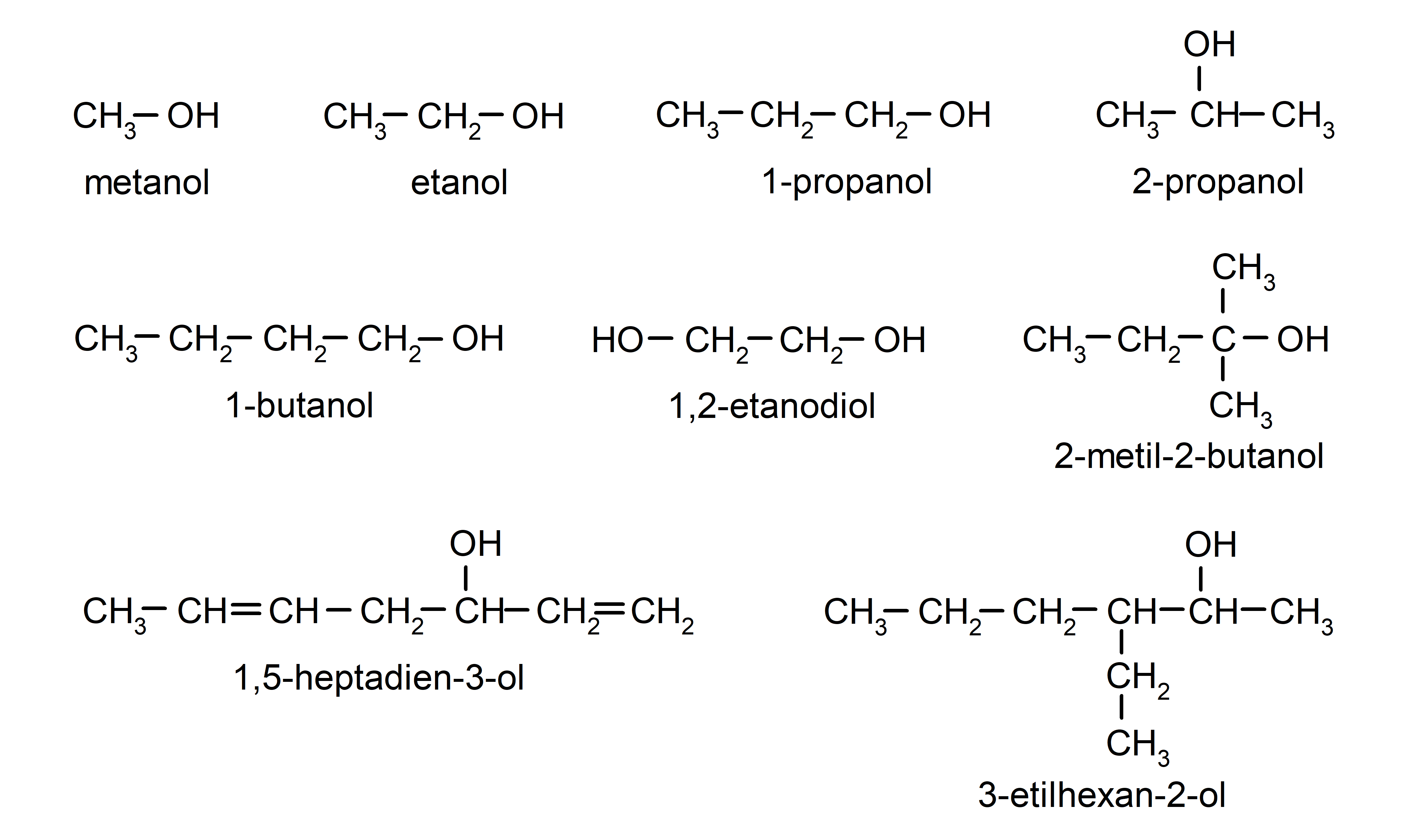
Ejemplos de alcoholes
- metanol
- etanol
- 1-propanol
- 2-propanol
- 1-butanol
- 3-etilhexan-2-ol
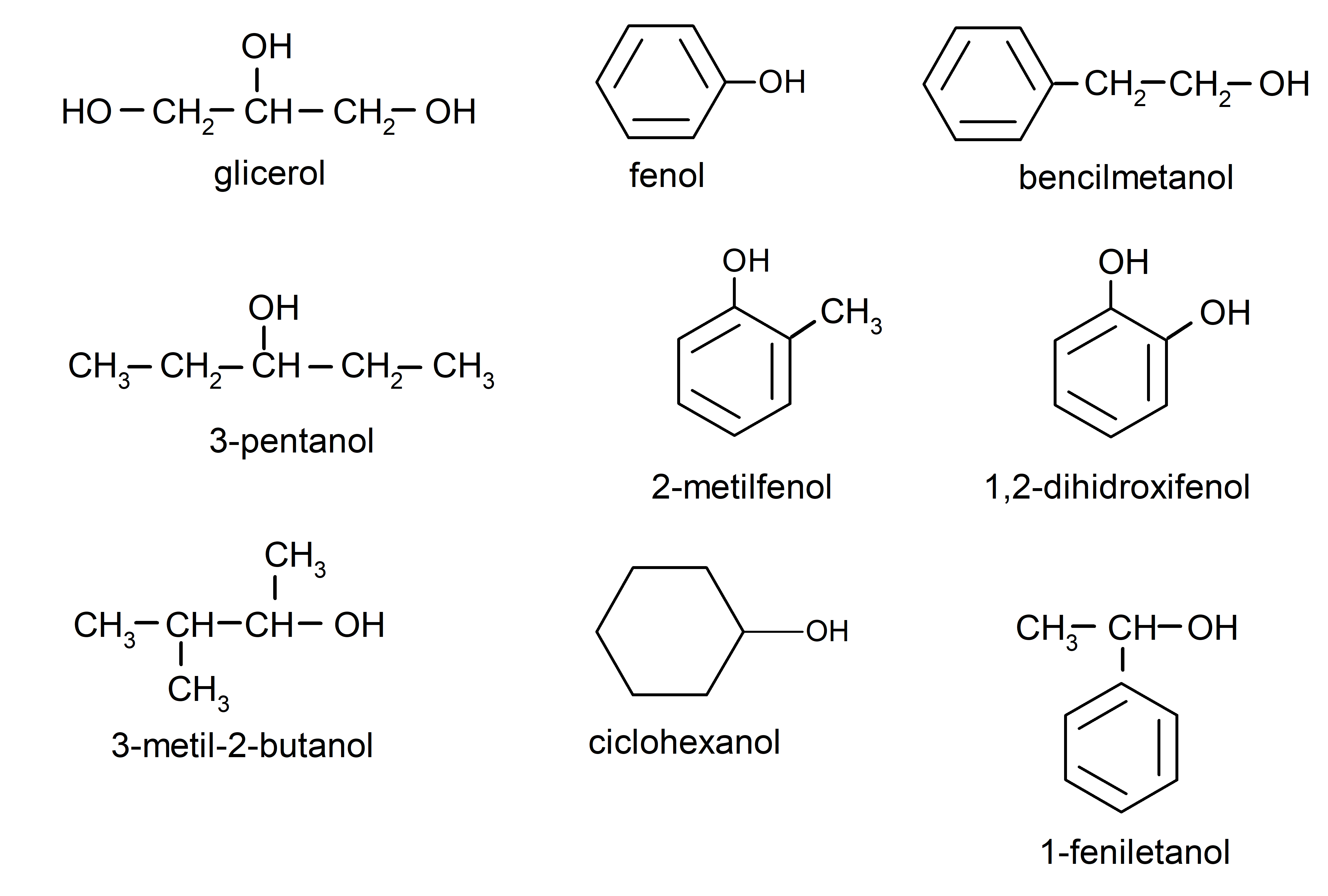
- glicerol
- fenol
- 2-metil-2-butanol
- 1,2-etanodiol
- 1,5-heptadien-3-ol
- 3-metil-2-butanol
- bencilmetanol
- 3-pentanol
- 2-metilfenol
- 1,2-dihidroxifenol
- cicloheaxnol
- 1-feniletanol
Usos de los alcoholes.
Los usos más comunes de los alcoholes son:
- Se utilizan como desinfectantes y antisépticos ya que frenan el crecimiento de algunos microorganismos o los destruyen. El etanol y el alcohol isopropílico son los más usados con este fin.
- Se emplean en la síntesis de diferentes compuestos químicos. El metanol, por ejemplo, se utiliza para obtener metanal (formaldehído).
- Se emplean para producir anticongelantes. El metanol es uno de los más utilizados con este fin.
- Se usan como disolventes en la industria farmacéutica. El etanol es uno de los más utilizados en este sentido.
- Se usan como disolventes de lacas, colorantes y tintas. El metanol es muy utilizado con este fin.
- Se emplean como combustible y existe una importante tendencia a sustituir parcialmente el uso de combustibles fósiles por el uso de bioetanol combustible.
- Se utilizan para fabricar resinas. El fenol es empleado en este sentido.
Peligros del consumo de alcohol
Aunque el consumo de alcohol hoy es socialmente aceptado, el abuso de esta sustancia genera dependencia y adicción.
El etanol es el alcohol presente en las bebidas alcohólicas, que cuando se consume en exceso afecta las habilidades cognitivas, y puede provocar enfermedades cardiovasculares, cirrosis hepática y cáncer.
Además, cuando se llega al grado de intoxicación alcohólica, es decir, estado de embriaguez, si la dosis del alcohol es muy alta, se puede producir un coma alcohólico, que puede llevar a parálisis respiratoria e incluso la muerte.
Sigue con:
¿Te fue útil esta información?
Sí No¡Genial! gracias por visitarnos :)