Geralmente, quando falamos sobre os estados da matéria, nos referimos a três grupos principais: sólido, líquido e gasoso (embora também exista o estado de plasma).
Os gases são um estado da matéria em que as moléculas interagem fracamente em uma determinada temperatura e pressão. Por exemplo: biogás, monóxido de carbono, hidrogênio, metano.
No estado gasoso, as moléculas não são coesas, portanto, os gases não constituem um corpo consistente com forma e volume definidos, como acontece com os sólidos. É por isso que os gases geralmente são imperceptíveis à visão, embora alguns sejam perceptíveis ao olfato.
Os gases se expandem pelo espaço disponível, ou seja, assumem a forma e o volume do recipiente em que estão contidos.
Mudanças de estado:
- A transformação do estado sólido para o estado gasoso por meio de um aumento brusco de temperatura e variação de pressão, sem passar primeiro pelo estado líquido, é chamada de sublimação.
- A transformação do estado líquido para o estado gasoso por meio de um aumento de temperatura é conhecida como vaporização.
- A transformação do estado gasoso para o estado líquido através da diminuição da temperatura é chamada de condensação.
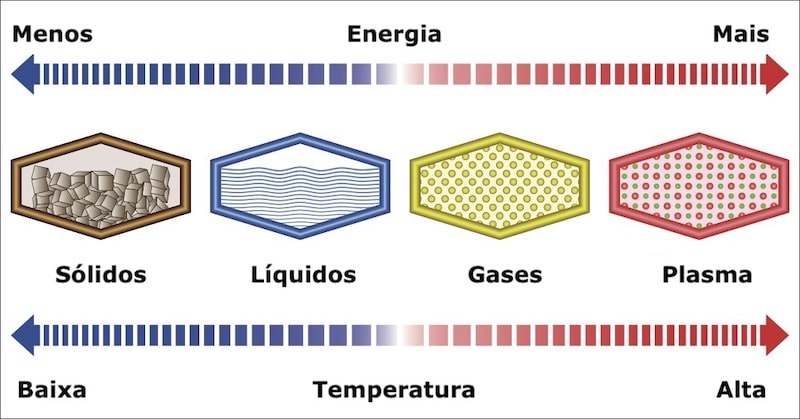
Características dos gases
- São muito fáceis de comprimir.
- Não têm forma definida.
- No estado gasoso, as moléculas estão em constante movimento, colidindo entre si e com as paredes do recipiente que as contém.
- Estas partículas se movem em velocidades diferentes de acordo com uma determinada temperatura.
- O movimento é mais rápido em temperaturas mais altas.
- As forças gravitacionais e de atração são insignificantes em comparação com a tendência de movimento das partículas que compõem os gases.
Pesquisa sobre gases e ar
Há muitos estudos e contribuições teóricas em física e química para analisar as características e o comportamento dos gases.
O ar (que quase todos os seres vivos precisam respirar) deve ter uma determinada composição, com uma quantidade suficiente de oxigênio. O dióxido de carbono também é um gás importante no ar; as plantas precisam dele para realizar o processo de fotossíntese.
Certos gases não devem exceder uma determinada proporção no ar; de fato, alguns gases de determinadas indústrias são altamente tóxicos e prejudiciais à saúde e podem poluir a atmosfera que respiramos (o monóxido de carbono é um exemplo disso).

Propriedades dos gases
Entre as principais propriedades dos gases, encontram-se:
- A expansão e a compressibilidade (os gases podem ser comprimidos pela ação de uma pressão externa e se expandir se essa pressão for liberada).
- A difusão (movimento de partículas de uma área de alta concentração para uma área de menor concentração) e a efusão (quando um gás está sob pressão em um recipiente e escapa para o exterior por meio de uma abertura).
- A densidade de um gás é bastante baixa.
O comportamento dos gases foi descrito por meio das leis dos gases formuladas por cientistas como Robert Boyle, Jacques Charles e Gay-Lussac. Estes físicos relacionaram parâmetros como volume, pressão e temperatura dos gases, que estão reunidos na chamada lei geral dos gases.
- Lei de Boyle. Estabelece que o volume de um gás é inversamente proporcional à pressão absoluta do recipiente que o contém em uma determinada temperatura e massa do gás.
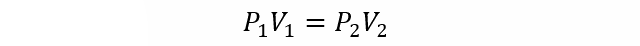
Onde:
P1 e P2 são as pressões inicial e final do gás, respectivamente.
V1 e V2 são os volumes inicial e final do gás, respectivamente.
- Lei de Charles. Estabelece que o volume de um gás é proporcional à sua temperatura em uma determinada pressão.
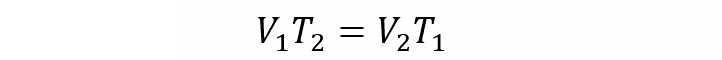
Onde:
T1 e T2 são as temperaturas inicial e final do gás, respectivamente.
V1 e V2 são os volumes inicial e final do gás, respectivamente.
- Lei de Gay-Lussac. Estabelece que a pressão de um gás é diretamente proporcional à temperatura quando o volume é constante.
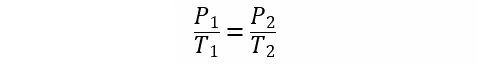
Onde:
T1 e T2 são as temperaturas inicial e final do gás, respectivamente.
V1 e V2 são os volumes inicial e final do gás, respectivamente.
Exemplos de matéria no estado gasoso

- Emissões que saem do escapamento de um carro em funcionamento.
- Os gases usados na refrigeração de geladeiras e condicionadores de ar.
- As nuvens no céu, compostas de vapor de água.
- O dióxido de carbono em refrigerantes carbonatados.
- O gás lacrimogêneo, que produz uma sensação desagradável no corpo humano.
- Balões de gás (cheios de gás hélio).
- O gás natural usado como combustível na rede doméstica.
- Biogás.
- A fumaça gerada pela queima de qualquer sólido.

- Monóxido de carbono
- Acetileno
- Hidrogênio
- Metano
- Butano
- Ozônio
- Oxigênio
- Nitrogênio
- Gás sulfídrico
- Hélio
- Argônio
- Continue com: Condensação
Esta informação foi útil para você?
Sim NãoGenial! Obrigado por nos visitar :)