Índice
Os fenômenos químicos (ou reações químicas) são aqueles em que se produzem mudanças na matéria, e se formam novas substâncias chamadas “produtos”, e ainda se decompõem outras chamadas “reagentes”. Por exemplo: podridão da madeira, combustão do papel, compostagem.
As reações químicas podem ser espontâneas (reações que ocorrem sem necessidade de energia ou catalisadores) ou não espontâneas (reações que necessitam de energia, catalisadores ou alguma intervenção externa para que ocorram). Muitas vezes, para que ocorra uma reação, é necessário que os reagentes tenham uma temperatura específica, um pH determinado, um valor de pressão estabelecido, etc.
Também pode ser fundamental controlar a velocidade em que ocorrem as reações químicas. Os catalisadores são substâncias adicionadas a uma reação química para aumentar a sua velocidade, enquanto os inibidores são substâncias que diminuem a velocidade das reações químicas. Outros fatores que afetam a velocidade de uma reação química são a temperatura, a pressão, a concentração dos reagentes e a natureza própria da reação.
- Veja também: Química orgânica e inorgânica
Tipos de fenômenos químicos
As reações químicas podem ser:
Reações inorgânicas. Envolvem compostos inorgânicos e podem ser classificados de acordo com:
- O sentido em que ocorre a reação.
- Reações reversíveis. Ocorrem em ambos os sentidos, de modo que os produtos podem se decompor e formar novamente os reagentes.
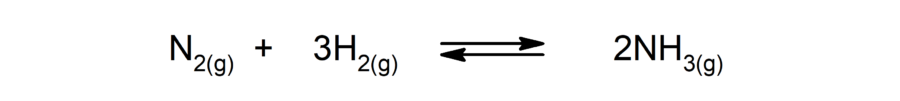
- Reações irreversíveis. Somente ocorrem em um sentido.

- O tipo de partícula que reage:
- Reações ácido-base. Ocorre transferência de íons H+.

- Reações de oxidação-redução. Um dos reagentes oxida (aumenta o seu número de oxidação), enquanto o outro é reduzido (diminui o seu número de oxidação). Nestas reações ocorre transferência de elétrons.
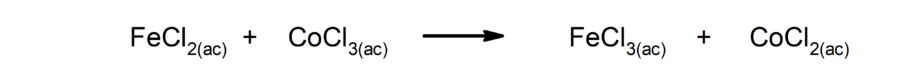
- A velocidade de reação
- Reações rápidas. Ocorrem em um tempo muito curto.
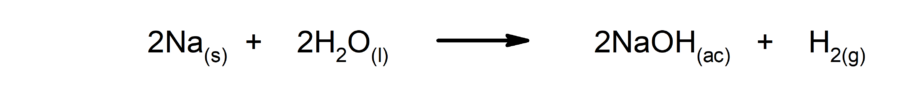
- Reações lentas. Demoram muito para serem completadas.
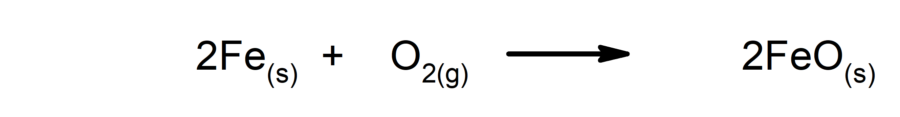
- A forma da energia que emite ou absorve.
- Reações exotérmicas. Ao ocorrerem, liberam calor.
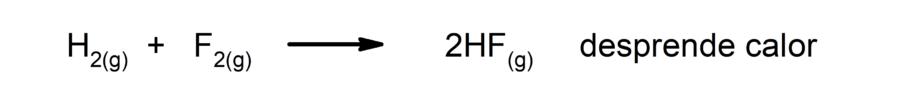
- Reações endotérmicas. Ao ocorrerem, absorvem calor.

- Reações exoluminosas. Ao ocorrerem, emitem luz.

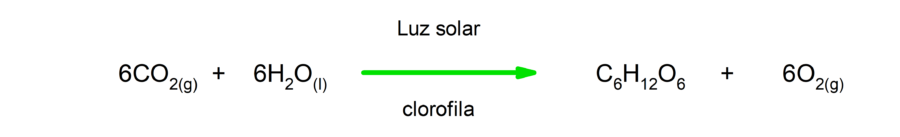
- Reações endoluminosas. Para ocorrerem, precisam de luz.
- O tipo de transformação
- Reações de síntese ou de adição. Duas substâncias são combinadas para formar uma nova substância.
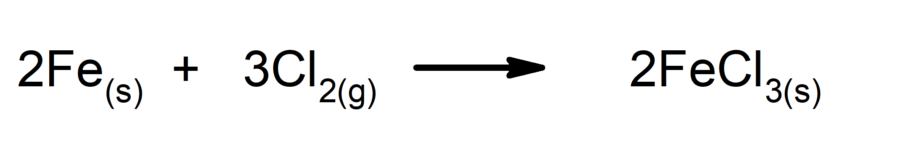
- Reações de decomposição. Uma ou mais substâncias se decompõem nos seus constituintes mais simples.
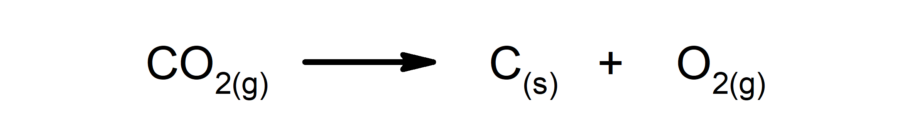
- Reações de deslocamento ou simples troca. Um elemento ou composto substitui outro em um composto, liberando-o.
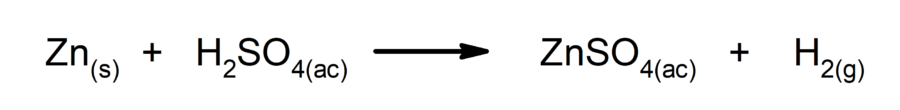
- Reações de dupla troca. Dois compostos trocam simultaneamente elementos ou compostos.

Reações orgânicas. São reações que envolvem compostos orgânicos. Têm muitas classificações com base no tipo de composto orgânico que reage e no tipo de reação que experimenta. Alguns exemplos são:
- Halogenação de alcanos. Substitui-se um hidrogênio de um alcano por um halogênio.
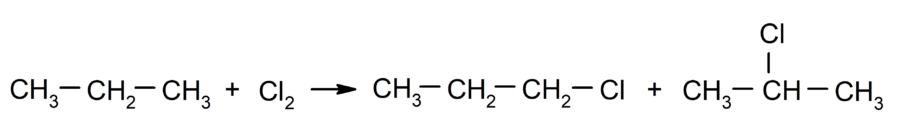
- Combustão de alcanos. Reage um alcano com o oxigênio para gerar dióxido de carbono e água, caso a combustão seja completa.
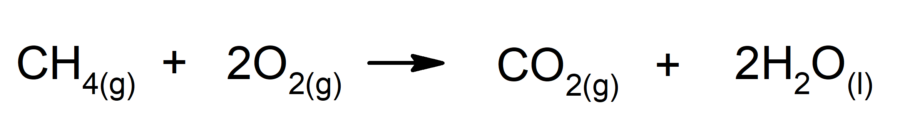
- Halogenação de alcenos. Substitui-se por halogênios um ou os dois hidrogênios dos carbonos que estão envolvidos na dupla ligação.
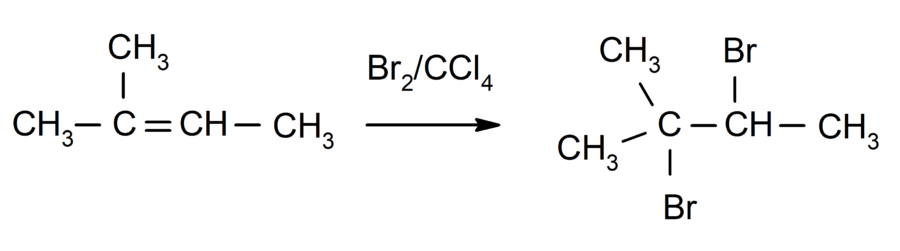
- Hidrogenação de alcenos. Adicionam-se hidrogênios aos carbonos envolvidos na dupla ligação para formar o alcano correspondente.
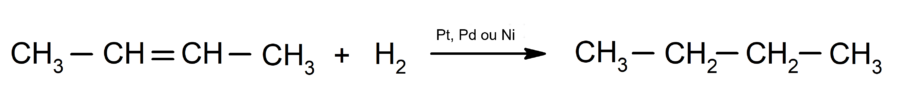
Importância dos fenômenos químicos
Muitos fenômenos químicos sustentam a vida dos seres vivos, como a digestão nos seres humanos e nos animais, a fotossíntese nas plantas e a respiração em ambos.
Outro processo químico muito importante, sobretudo na vida dos microrganismos, é a fermentação, que é geralmente utilizada na fabricação de alimentos como queijos, iogurtes, vinhos e cervejas.
Todo o crescimento e desenvolvimento de um ser vivo envolve reações químicas que ocorrem nele, às vezes estimuladas por determinadas condições ambientais.
Exemplos de fenômenos químicos
Ao nosso redor existem numerosos casos de fenômenos químicos ou de processos que os incluem:
- Podridão da madeira
- Combustão de papel
- Resistência a antibióticos de bactérias
- Leite que azeda
- Desinfecção de uma ferida com álcool
- Uso de sal de frutas para combater a acidez do estômago
- Combustão de uma vela
- Coagulação do sangue
- Fadiga muscular após exercício intenso
- Morte de insetos por inseticidas
- Obtenção de queijo roquefort
- Obtenção de sidra
- Obtenção de iogurte
- Compostagem
- Silagem
- Obtenção de bioetanol a partir do melado
- Latas de conservas com inchaço duro
- Ovo podre
- Oxidação de uma grade
- Obtenção de biodiesel a partir do azeite de dendê
Os fenômenos químicos na indústria
Certos fenômenos químicos também são cruciais na indústria. Para começar, a combustão de hidrocarbonetos (como a gasolina, o gasóleo ou o querosene) produz energia para fazer funcionar as máquinas que operam um sem número de processos industriais.
Por sua vez, a indústria siderúrgica, papeleira, de plásticos, de materiais de construção, de tintas, de fármacos, de produtos para o agro, etc., têm como base diversos fenômenos químicos como a galvanização, a eletrólise e muitos outros.
A geração de novas fontes de energia (como o biodiesel e o bioetanol) também se baseia neste tipo de fenômenos.
A transformação da energia
Nos fenômenos químicos é comum que haja transformação da energia. Por exemplo, quando a energia química contida nas ligações de uma determinada molécula é transformada em energia elétrica ou liberada como calor (isto ocorre nos fenômenos exotérmicos, como quando se mistura ácido clorídrico com zinco), existe uma transformação de energia. O mesmo acontece quando a energia luminosa é captada e transformada em energia química.
Alguns processos químicos precisam de calor para serem realizados e são chamados de “endotérmicos”. Outros, requerem a presença de catalisadores ou cofatores.
Continue com:
Esta informação foi útil para você?
Sim NãoGenial! Obrigado por nos visitar :)