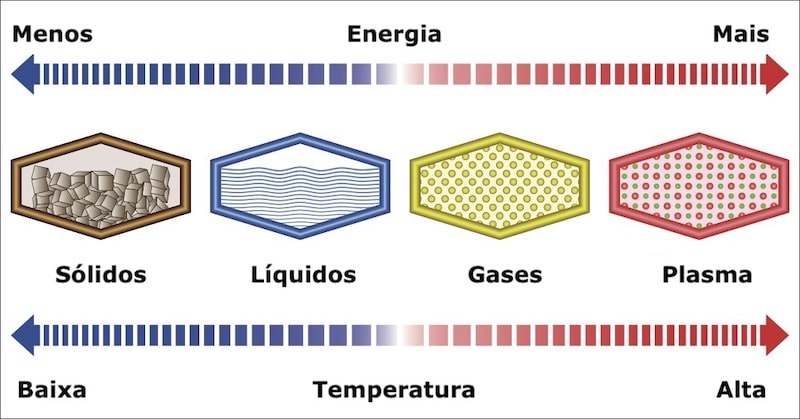
São denominados líquidos os produtos e as substâncias que se encontram neste estado da matéria. Há três estados possíveis da matéria: sólido, líquido e gasoso (e o plasma é atualmente definido como o quarto estado da matéria). Estes estados são diferenciados pelo grau de coesão das moléculas que os compõem. Por exemplo: água, petróleo, glicerina.
No estado líquido, as forças de atração entre as moléculas são mais fracas do que nos sólidos, porém mais fortes do que nos gases. As moléculas se movem e colidem umas com as outras, vibrando e deslizando umas sobre as outras.
Nos líquidos, o número de partículas por unidade de volume é muito alto, de modo que as colisões e o atrito entre as partículas são muito frequentes. O fato de uma substância estar em um estado líquido, sólido ou gasoso depende principalmente da temperatura e de sua pressão de vapor. Nas regiões temperadas do mundo, a água, por exemplo, está no estado líquido.
Nos líquidos, as moléculas podem se mover e colidir umas com as outras, ou seja, elas ficam relativamente próximas umas das outras. À medida que a temperatura de um líquido aumenta, a quantidade de movimento de suas moléculas individuais também aumenta.
Consequentemente, os líquidos podem fluir para assumir a forma de seu recipiente, mas não podem ser facilmente comprimidos porque as moléculas já estão firmemente unidas. Por isso, os líquidos não têm uma forma fixa, mas têm um volume definido. Os líquidos estão sujeitos aos processos de expansão e contração, dependendo da temperatura e da pressão aplicadas a eles.
As propriedades dos líquidos
Entre as principais características das substâncias líquidas está o ponto de ebulição, ou seja, a temperatura na qual entram em ebulição e se tornam gasosas. Isso é dado pela pressão de vapor, que é igual à do meio que envolve o líquido.
- Tensão superficial. Dada pelas forças de atração de suas partículas em todas as direções dentro do líquido.
- Viscosidade. Representa a força oposta de um fluido quando ele se move devido a uma diferença de pressão (isso só ocorre em líquidos em movimento).
- Capilaridade. Descreve a facilidade que os líquidos têm para subir em tubos de pequeno diâmetro (capilares), nos quais a força de coesão é superada pela força de adesão.
- Fluidez. É a capacidade de um líquido de passar por um orifício que está no mesmo nível do recipiente em que se encontra.
Exemplos de líquidos
A seguir, exemplos de substâncias líquidas a 25 °C:
- Água
- Petróleo
- Querosene
- Álcool etílico
- Metanol
- Éter de petróleo
- Clorofórmio
- Benzeno
- Ácido sulfúrico
- Ácido clorídrico
- Glicerina
- Acetona
- Acetato de etilo
- Ácido fosfórico
- Tolueno
- Ácido acético
- Leite
- Óleo comestível composto
- Álcool isoamílico
- Óleo de girassol
Continue com:
Esta informação foi útil para você?
Sim NãoGenial! Obrigado por nos visitar :)