A combinação química de certos catiões com certos aniões origina o que em química se denominam sais. Na natureza existem numerosos sais dissolvidos nos mares ou precipitados, formando minerais de média ou alta complexidade. Em geral, estes são sais minerais, ou seja, compostos por elementos inorgânicos. Por exemplo: oxalato de cálcio, cloreto de sódio, sulfato de cobre.
Estima-se que um litro de água do mar contenha, em média, entre 33 e 39 gramas de sal. Muitos sais têm utilizações domésticas importantes, outros são essenciais para a indústria ou para a construção.
Os sais apresentam frequentemente uma estrutura cristalina, embora se encontrem dissolvidos e ionizados nos meios líquidos. São fundamentais para os seres vivos, ajudam a manter a homeostase celular e o equilíbrio osmótico pela sua capacidade de absorver moléculas de água.
No entanto, um excesso de sais pode resultar em sérios problemas de saúde, como hipertensão arterial. Alguns seres vivos necessitam de sais minerais para formar estruturas externas de proteção, como conchas e carapaças. Além disso, os ossos de todos os vertebrados são compostos por sais.
- Veja também: Moléculas orgânicas e inorgânicas
De onde se obtém o sal?
Na natureza, muitos sais se concentram nas salinas, ou seja, em lagos superficiais cujos sedimentos são compostos por sais. À medida que o sol se evapora na água, os sais se acumulam.
São famosos na América, por exemplo, as salinas de Uyuni, na Bolívia ou as de Atacama, no Chile. Também há mares ou lagos endorreicos muito ricos em sais: o exemplo mais conhecido é o do Mar Morto, localizado a 416,5 metros abaixo do nível do mar, especialmente rico em sais de cálcio, magnésio, potássio e bromo. O teor salino do Mar Morto é de cerca de 28%.
Os sais orgânicos são o resultado da reação entre um alcalino, como hidróxido de sódio ou de potássio, e algum ácido graxo. Este processo é conhecido como saponificação. Os sais orgânicos têm frequentemente propriedades detergentes, por isso são frequentemente a base de vários produtos de limpeza.
Existem várias reações químicas que levam à formação de sais, como por exemplo:
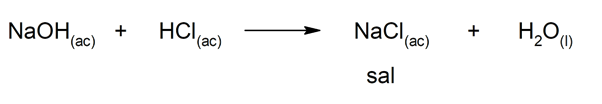
- Reação entre um metal e um não metal:
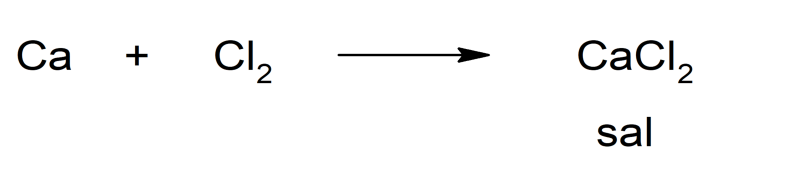
- Reação entre um metal e um ácido:
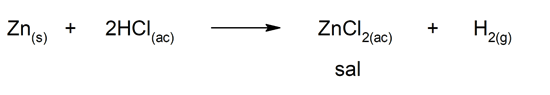
- Reação de saponificação:
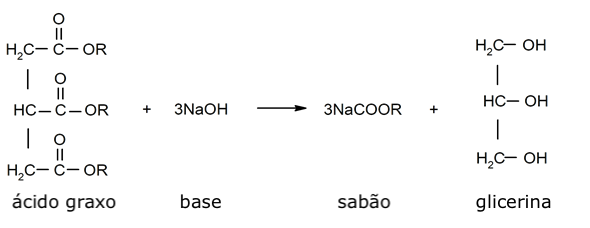
Exemplos de sais
| Taurocolato de sódio | Cloreto de benzalcônio |
| Carbonato de cálcio (CaCO3) | Oxalato de cálcio |
| Brometo de potássio (KBr) | Bicarbonato de sódio NaHCO3 |
| Sulfato de magnésio (MgSO4) | EDTA dissódico |
| Cloruro de sódio (NaCl) | Carbonato de magnésio (MgCO3) |
| Hipoclorito de sódio (NaClO) | Sulfato de cobre (CuSO4) |
| Fosfato tricálcico (Ca3(PO4)2) | Citrato de potássio |
| Cloreto de amônia (NH4Cl) | Sulfato de amônia ((NH4)2SO4) |
| Lauril sulfato de sódio | Telureto de sódio (Na2TeO3) |
| Sulfonato de 4-dodecilbenzeno sódico | Permanganato de potássio (KMnO4) |
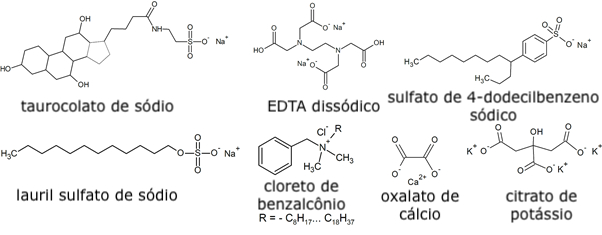
Continue com:
Esta informação foi útil para você?
Sim NãoGenial! Obrigado por nos visitar :)