As soluções são um tipo de mistura formada por componentes que não reagem quimicamente entre si, mas que podem alterar suas propriedades físicas quando passam a fazer parte da solução. Por exemplo: humo, amálgama, café com leite.
Para que uma mistura seja uma solução, deve ser homogênea e uniforme, ou seja, os componentes misturados devem ser indistinguíveis a olho nu, além de que a proporção entre o soluto (substância que aparece em quantidades menores) e o solvente (substância que aparece em quantidades maiores) deve se manter aproximadamente invariável em qualquer volume retirado da solução.
A proporção do soluto na solução ou no solvente é chamada de “concentração” e, normalmente, uma solução pode ser preparada usando várias concentrações de soluto.
- Veja também: Propriedades físicas e químicas da matéria
Tipos de soluções
As soluções podem ser classificadas de acordo com seu estado de agregação. É importante mencionar que as soluções podem ser formadas entre substâncias que, antes de serem misturadas, estão em qualquer um dos diferentes estados de agregação da matéria: sólido, gasoso ou líquido.
Existem soluções em praticamente todos os estados de agregação. Geralmente, o estado de agregação da solução é determinado pelo estado de agregação do solvente.
Os tipos de soluções são:
- Solução de gases em gases (gasosa). Por exemplo: o ar que respiramos.
- Solução de sólidos em gases (gasosa). Por exemplo: a poeira dissolvida no ar.
- Solução de líquidos em gases (gasosa). Por exemplo: o vapor de água no ar.
- Solução de sólidos em líquidos (líquida). Por exemplo: o sal de mesa (NaCl) dissolvido em água.
- Solução de líquidos em líquidos (líquida). Por exemplo: o etanol (CH3CH2OH) dissolvido em água.
- Solução de gases em líquidos (líquida). Por exemplo: o oxigênio (O2) dissolvido em água.
- Solução de sólidos em sólidos (sólida). Por exemplo: as ligas metálicas, como o bronze (liga de cobre e estanho).
- Solução de gases em sólidos (sólida). Por exemplo: o gás hidrogênio dissolvido em paládio.
- Solução de líquidos em sólidos (sólida). Por exemplo: os amálgamas, que são a solução de mercúrio em outros metais sólidos.
Além disso, é comum que a presença de moléculas de soluto em um solvente altere as propriedades do próprio solvente. Por exemplo, os pontos de fusão e ebulição de dois compostos mudam quando esses compostos são misturados, e suas densidades e cores também podem mudar.
Lei de Raoult
O cientista francês François Marie Raoult estudou o comportamento dos componentes em soluções e propôs a Lei de Raoult. Esta lei afirma que a pressão parcial de vapor de cada componente na mistura de vapores que envolve uma solução líquida ideal é igual à pressão parcial de cada componente puro vezes sua fração molar na solução.
Considera-se uma solução ideal aquela em que as espécies químicas são muito semelhantes, de modo que não se considera variação na energia das interações entre elas. A equação fundamental da Lei de Raoult é:
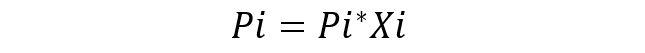
Onde:
- Pi é a pressão parcial do componente i na mistura gasosa que envolve a solução.
- Pi* é a pressão do componente i.
- Xi é a fração molar do componente i na solução.
Exemplos de soluções na vida diária
As soluções são misturas que estão presentes em uma variedade de ambientes, na natureza, nas residências e nas indústrias. Algumas das mais comuns são:
- Ar (gás em gás). É uma solução composta de gases, incluindo nitrogênio e oxigênio, que estão presentes na atmosfera.
- Fumaça (sólido em gás). É uma solução na qual o ar atua como solvente e que é gerada após a combustão.
- Ligas entre metais (sólido em sólido). São misturas que ocorrem entre metais, por exemplo, o duralumínio é uma liga composta de alumínio, cobre, manganês, magnésio e silício.
- Poeira do ar atmosférico (sólido em gás). É uma solução formada pela presença de sólidos (partículas de poeira) no gás.
- Aço (sólido em sólido). É uma liga de ferro e carbono, com uma proporção muito maior do primeiro, usada na fabricação de máquinas e ferramentas.
- Bebida carbonatada (gás em líquido). É comumente chamada de “refrigerante” e é uma dissolução de gases (como o ácido carbônico) em um líquido (água).
- Amálgama (líquido em sólido). É uma liga de mercúrio que é dissolvida em certos metais, como ouro ou prata, e é frequentemente usada em odontologia.
- Petróleo refinado (líquido em líquido). É uma solução formada pela combinação de elementos (sendo o carbono o principal deles) e é usada como combustível.
- Butano no ar (gás em gás). É a solução entre o alcano butano e o ar. O butano é um composto químico gasoso que pode ser armazenado em tubos e usado como combustível.
- Oxigênio na água do oceano (gás em líquido). É a solução que se dá entre a água e o oxigênio permitindo o desenvolvimento da vida aquática.
- Bebida alcoólica (líquido em líquido). É uma solução de etanol e sucos de frutas.
- Café com leite (líquido em líquido). Café com leite (líquido em líquido).
É uma solução em que o café dissolvido em água recebe leite, resultando em uma transformação de sua cor e sabor. - Smog (gases em gases). É uma dissolução que ocorre a partir da introdução de gases que não são próprios da atmosfera, o que induz a uma transformação do ar.
- Sal na água (sólido em líquido). É uma solução líquida e homogênea que se obtém quando o sal é dissolvido em água.
- Sangue (líquido em líquido). É uma solução resultante da união do principal componente do sangue (plasma) com outros elementos, como as células vermelhas do sangue.
- Amônia em água (líquido em líquido). É uma solução de amônia e água (que também pode ser feita de um gás para um líquido) usada em muitos produtos de limpeza.
- Ar com resquícios de umidade (líquido no gás). É a dissolução que se dá quando o vapor de água está presente no ar devido ao aumento da temperatura.
- Suco em pó (sólido em líquido). É uma solução que se obtém quando o suco instantâneo em pó é dissolvido em água, gerando um líquido colorido.
- Hidrogênio em paládio (gás em sólido). É a solução obtida quando o hidrogênio é dissolvido em alguns metais, como o paládio.
- Vírus transportados pelo ar (sólido em gás). É uma solução que ocorre quando unidades muito pequenas de um sólido são transportadas por um gás.
- Mercúrio em prata (líquido em sólido). É uma das chamadas “amálgamas”.
- Chá (sólido em líquido). É uma solução obtida quando um sólido de dimensões muito pequenas (os grânulos do sachê de chá) é dissolvido em água.
- Aqua régia (líquido em líquido). É uma composição de ácidos que permite dissolver diferentes metais, como o ouro.
- Bronze (sólido em sólido). É a liga entre o cobre e o estanho usada para fazer utensílios, joias, em indústrias como a de mineração e nos setores de transporte ferroviário e naval.
- Limonada (líquido em líquido). É uma solução de suco de limão que se dissolve em água.
- Água oxigenada (líquido em líquido). É uma solução de peróxido de hidrogênio (H2O2) em água usada para desinfetar ferimentos e na indústria de cosméticos.
- Resfriamento com gelo (sólido em líquido). É uma solução que ocorre quando o gelo é introduzido no líquido e o resfria, enquanto o dissolve.
- Soro fisiológico (sólido em líquido). É uma solução composta de cloreto de sódio e água, que atua como solvente e é usada para hidratação de pacientes.
- Detergente (líquido em líquido). É uma solução usada para a limpeza de louças, sendo composta por elementos como água, álcool e sulfonato de sódio.
- Vitamina (sólidos em líquidos). É uma substância obtida pela combinação de alimentos sólidos, como frutas, e líquidos, como água ou leite.
- Água com açúcar (sólidos em líquido). É uma solução feita de água e grãos de açúcar.
- Leite com achocolatado (sólidos em um líquido). É uma solução líquida obtida pela mistura de cacau em pó ou barras de chocolate com leite.
- Perfume. É uma solução que surge da mistura de diferentes substâncias, como água, álcool, corantes, entre outras.
- Álcool e água (líquido em líquido). É uma solução líquida obtida pela mistura de álcool e água. Essa solução é frequentemente usada para desinfecção de superfícies.
- Água do mar. É uma solução composta de sais, como cloro, magnésio e sódio, dissolvidos em água.
- Aço inoxidável. É uma liga de ferro, carbono e cromo que se caracteriza por sua resistência e não oxidação. É usado na fabricação de utensílios de cozinha, eletrodomésticos, móveis, máquinas e instrumentos cirúrgicos.
- Latão. É uma liga de cobre e zinco empregada em serralheria, joalheria, componentes elétricos, entre outros.
- Enxaguante bucal. Solução líquida usada para higiene bucal, composta geralmente de componentes como água, álcool e óleos, e que ajuda a eliminar bactérias.
- Limpador de piso. É uma solução líquida empregada na limpeza de pisos e outras superfícies e é composta de água, álcool e outros elementos que ajudam a matar vírus e bactérias.
- Vinagre. É uma solução líquida composta de água e ácido acético, usada para temperar alimentos e também pode ser usada para limpar e desinfetar superfícies.
- Continue com: Coloides
Esta informação foi útil para você?
Sim NãoGenial! Obrigado por nos visitar :)