Índice
Las sales binarias (sales neutras) se forman cuando se combinan un metal y un no metal. Son compuestos químicos formados por solo dos elementos químicos. Por ejemplo: cloruro de sodio (NaCl) y bromuro de potasio (KBr).
Ejemplos de sales binarias
- Cloruro de sodio (NaCl)
- Cloruro de hierro (II) (FeCl2)
- Cloruro de hierro (III) (FeCl3)
- Sulfuro de cobalto (II) (CoS)
- Sulfuro de cobalto (III) (Co2S3)
- Sulfuro de plomo (II) (PbS)
- Sulfuro de plomo (IV) (PbS2)
- Cloruro de calcio (CaCl2)
- Fluoruro de sodio (NaF)
- Cloruro de litio (LiCl)
- Cloruro de estroncio (SrCl2)
- Cloruro de bario (BaCl2)
- Cloruro de aluminio (AlCl3)
- Sulfuro de magnesio (MgS)
- Cloruro de rubidio (RbCl)
- Bromuro de calcio (CaBr2)
- Sulfuro de potasio (K2S)
- Bromuro de magnesio (MgBr2)
- Sulfuro de zinc (Zn2S)
- Bromuro de litio (LiBr)
- Cloruro de níquel (NiCl2)
- Cloruro de uranio (III) (UCl3)
- Bromuro de plata (AgBr)
- Yoduro de plata (AgI)
- Bromuro de potasio (KBr)
Nomenclatura de las sales binarias
Según la Nomenclatura Tradicional, las sales binarias se nombran escribiendo el nombre del elemento no metálico con la terminación -uro. Por otra parte, el nombre del elemento metálico se escribe según su estado de oxidación:
- Para el menor estado de oxidación, se escribe con la terminación -oso. Por ejemplo: el cloruro ferroso (FeCl2), donde el hierro tiene estado de oxidación 2+.
- Para el mayor estado de oxidación, se escribe con la terminación -ico. Por ejemplo: el cloruro férrico (FeCl3), donde el hierro tiene estado de oxidación 3+.
Según la Nomenclatura Sistemática, las sales binarias se nombran escribiendo el nombre del elemento no metálico con un prefijo que indica la cantidad de átomos de este elemento en el compuesto. Además, se coloca la terminación -uro al nombre del elemento no metálico. Luego, se coloca el nombre del elemento metálico. Por ejemplo: el dicloruro de magnesio (MgCl2) y el tricloruro de hierro (FeCl3).
Según la nomenclatura de Stock, las sales binarias se nombran escribiendo el nombre del elemento no metálico con la terminación -uro. Luego, se coloca el nombre del elemento metálico seguido de su estado de oxidación escrito en números romanos y entre paréntesis. Por ejemplo: el cloruro de hierro (II) (FeCl2) y el sulfuro de cobalto (III) (Co2S3).
Aplicaciones de las sales binarias
- Se utilizan como refrigerantes en la industria alimentaria y farmacéutica. Por ejemplo: el cloruro de calcio (CaCl2).
- Se utilizan para tratar superficies metálicas contra la corrosión. Por ejemplo: el fluoruro de sodio (NaF).
- Se utilizan para regular la humedad en la industria del papel y la construcción. Por ejemplo: el cloruro de calcio (CaCl2).
- Se emplean en la industria del vidrio para eliminar impurezas. Por ejemplo: el tetracloruro de silicio (SiCl4).
- Se usan como ingredientes de cocina. Por ejemplo: el cloruro de sodio (NaCl).
Propiedades físicas de las sales binarias
- Tienen puntos de fusión elevados debido a que están formadas por enlaces iónicos.
- Conducen la corriente eléctrica cuando están disueltas o fundidas.
- Las sales más comunes tienen baja dureza.
- No son compresibles.
- La mayoría puede disolverse en agua.
¿Cómo se obtienen las sales binarias?
Las sales binarias se pueden obtener mediante algunas de las siguientes reacciones químicas:
Reacción entre un metal y un no metal. Por ejemplo: la reacción entre el sodio (Na) y el dicloro (Cl2) produce cloruro de sodio (NaCl).
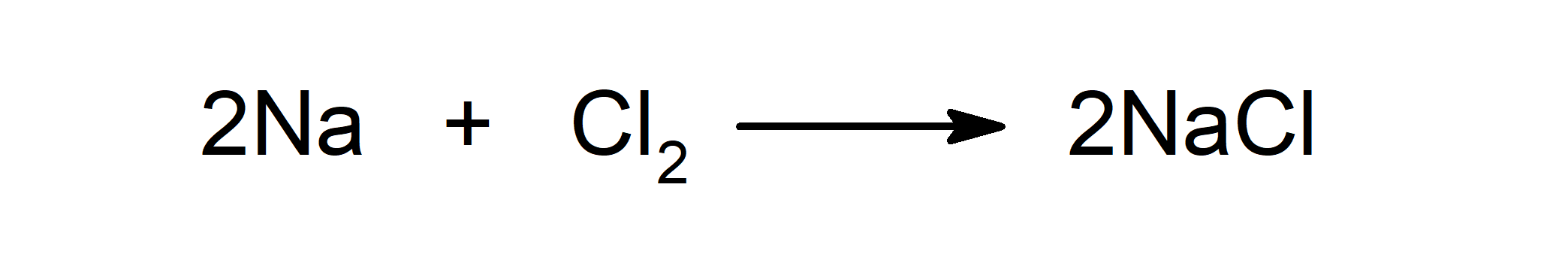
Reacción entre un metal y un ácido. Por ejemplo: la reacción entre el potasio (K) y el ácido clorhídrico (HCl) produce cloruro de potasio (KCl) y dihidrógeno (H2).

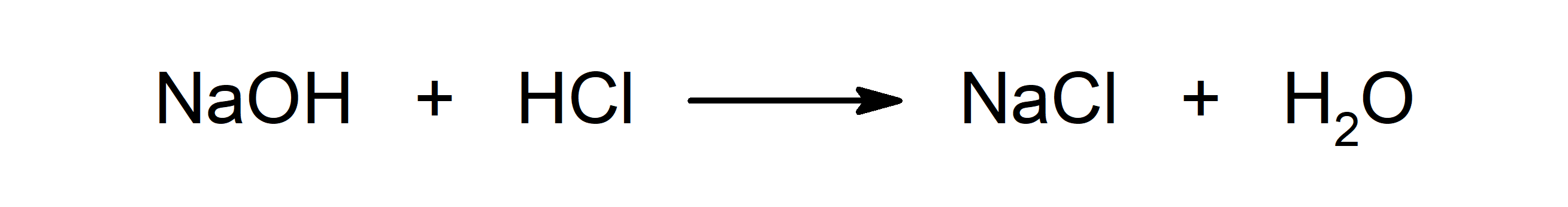
Reacción entre un ácido y una base. Por ejemplo: la reacción entre el ácido clorhídrico (HCl) y el hidróxido de sodio (NaOH) produce cloruro de sodio (NaCl) y agua (H2O).
Sigue con:
¿Te fue útil esta información?
Sí No¡Genial! gracias por visitarnos :)